|
2011年湖北荆州市中考化学模拟试题 湖北省洪湖市实验中学 陈 新 可能用到的相对原子质量:C-12 H-1 O-16 Fe-56 Ba-137 Cl-35.5 Cu-64 S-32 一、选择题(本大题包括15小题。每小题1分,共15分。每小题只有一个符合题意的选项,请将符合题意选项的序号填写在下面的答题栏内。) 1.下列变化属于化学变化的是 A.潮涨潮落 B.灯泡发光 C.瓦斯爆炸 D.干冰升华 2.下列关于氧气的说法中,错误的是 A.氧气用于炼钢,目的是除去生铁中多余的碳和其他杂质 B.氧气可以支持燃烧,说明氧气具有可燃性 C.氧气可以供给呼吸,是因为和体内物质反应而释放能量,维持生命活动 D.夏天鱼池内放增氧泵,是因为温度升高,氧气在水中溶解量减少 3.雄伟壮观的国家大剧院主体建筑表面安装了近2万块钛(Ti)金属板。已知Ti原子核内有22个质子,则下列叙述正确的是 A.Ti可以表示一个钛原子 B.钛原子的相对原子质量为22 C.TiO2中含有氧分子 D.CaTiO3属于金属氧化物 4.碘片是一种可以减少甲状腺对放射性碘131吸收的药物,其主要成分是碘化钾。碘化钾(KI)中碘元素的化合价是 A.0 B.-1 C.+1 D.+2 5.自然科学的发展使我们生活变得丰富多彩。通过化学的学习,你觉得下列情况中不可能实的是 A.通过化学反应使水直接变成汽油 B.用肥皂水区分硬水和软水 C.用人工的方法合成结晶牛胰岛素 D.用高温煅烧法除去氧化钙中混有的碳酸钙 6.从下列图片中不能获取的信息是  A.分子之间有间隔 B.硅原子是由原子核和电子构成的 C.构成物质的粒子有分子、原子和离子 D.受热水分子运动速率加快 7.芜湖铁画是中国工艺美术百花园中的一朵奇葩。它以钢材为主料,经锻打、焊接、酸洗、上漆等多道工艺制成。下列关于铁画的叙述不正确的是 A.铁画应悬挂在干燥的环境中 B.所用材料上的铁锈可用稀盐酸清洗掉 C.给打制成型的铁画喷漆既美观又可以防锈蚀 D.所用的主要材料──低碳钢,有较好的锻轧性能,它不属于铁的合金 8.下列说法正确的是 A.氧离子的电子数少于氧原子的电子数 B.氢氧化钠能去除油污,可直接用做厨房的清洁剂 C.把100 g12%的氯化钠溶液配制成6%的氯化钠溶液,需加水100 g D.100 g9.8%硫酸溶液与100 g20.8%的氯化钡溶液反应,所得溶液质量为200 g 9.下列基本的实验操作不正确的是    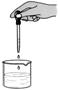 A.液体体积读数 B.熄灭酒精灯 C.检查气密性 D.滴加液体 10.碳家族中,C60的分子结构形似足球。关于C60的说法中,错误的是 A.它是一种单质 B.每个C60 分子由60个碳原子构成 C.它与金刚石是同一种物质 D.它完全燃烧后的产物是CO2 11.食用鱼、鸡蛋、瘦肉等食品,主要是为人体补充 A. 蛋白质 B.维生素 C.油脂 D.糖类 12.物质与水发生的复分解反应称为水解反应。例如:Al2S3+6H2O=2Al(OH)3↓+3H2S↑。根据上述观点,下列说法中不正确的是 A.NaF的水解产物是NaOH和HF B.CaO2的水解产物是Ca(OH)2和H2O2 C.Mg3N2水解产物是M g(OH)2和NH3 D.PCl3的水解产物之一是PH3 13.氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是 A.NH4Cl与KCl:观察外观 B.NH4HCO3与KCl:加水 C.K2SO4与Ca3(PO4)2:闻气味 D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味 14.了解安全知识,可以更好地保护人身和财产安全。下列做法不正确的是 A.发现燃气泄漏应立即开窗通风关阀门 B.用亚硝酸钠腌渍鱼肉和蔬菜 C.霉变的大米、瓜子、花生等不能食用 D.室内起火应压低身体逃离火场 15.由C、H两种元素组成的化合物叫烃,碳原子数在4及以下的烃在常温常压下通常为气体。常温常压时,烃C2H4和另一种烃组成的混合气体中碳元素的质量分数为87%,则混入的烃可能是 A.CH4 B.C2H2 C.C2H6 D.C8H8 二、填空题(本大题包括5小题,共16分。) 16.(2分)用化学符号表示:(1)2个氢原子:________。 (2)3个铝离子:________。 17.(3分)实验室新进一批浓硝酸,化学兴趣小组为研究该试剂的保存方法,开展相关探究。请根据要求回答问题:(1)打开盛装浓硝酸的试剂瓶,立即观察到瓶口有白雾产生。据此可知,浓硝酸具有_______________(填一条物理性质)。(2)将少量浓硝酸置于试管中,采用强光照射或者稍加热,立即观察到溶液上方有红棕色气体(NO2)产生。据此现象可推知浓硝酸具有_____________________________(填一条化学性质)。(3)通过上述实验可知,实验室应如何保存浓硝酸?________________________________________________________。 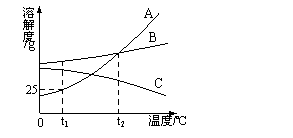 18.(3分)右图是A、B、C三种固体物质在水中的溶解度曲线,据图回答: 18.(3分)右图是A、B、C三种固体物质在水中的溶解度曲线,据图回答:(1) 有t1℃时A的饱和溶液80 g,其中A的质量为_________。 (2)当A物质中混有少量B物质时,通常可采用____________________的方法提纯A。 (3) 将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃后(升温过程中溶剂量不变),三种溶液中溶质的质量分数由大到小的顺序是____________(填序号)。  19.(4分)A、B、C、D、E分别是稀硫酸、氢氧化钠溶液、硫酸铜溶液、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“──”两端的物质在一定条件下可以反应。请回答: 19.(4分)A、B、C、D、E分别是稀硫酸、氢氧化钠溶液、硫酸铜溶液、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“──”两端的物质在一定条件下可以反应。请回答:(1)C中存在的粒子有__________________(填化学符号)。 D和E反应的化学方程式为______________________________。 (2)上述各物质间的反应均可用“甲+乙→丙+丁”表示,其中不属于四种基本反应类型,但能用上式表示的一个化学方程式是____________________。 (3)若B、C、D、E都不变,五种物质之间的关系也不变,A还可能是_____(填化学式)。 20.(4分)某校实验室仅提供了以下实验药品:锌片、镁片、铜片、稀盐酸、硝酸银溶液。该校九年级化学研究性学习小组的同学们为了探究锌、铜、镁、银的金属活动性顺序,设计了如下实验方案:①将大小一样的锌片和镁片分别加入到溶质的质量分数相同的稀盐酸中;②将铜片加入到硝酸银溶液中,铜片上出现银白色物质;③将金属片A放入到溶液B中。 (1)实验①的现象是________________________________________________; (2)实验②中发生反应的化学方程式是_________________________________; (3)实验③中的金属片A是__________,溶液B是_______________________。 三、实验题(本大题包括3小题,共12分。) 21.(3分)某校化学兴趣小组的同学按下列实验步骤进行粗盐提纯,请回答下列问题:  (1)操作①、②、③依次为下图中的(填字母)_____________。  A B C (2)若NaCl的产率偏低( A.过滤时滤纸有破损 B.蒸发时有固体溅出 C.溶解含有泥沙的粗食盐时,加入的水量不足 22.(4分)在初中化学学习中我们掌握了氧气、氢气、二氧化碳的制取和收集方法。某校化学兴趣小组的同学,按规范的操作要求,运用合理的装置在实验室制取了这些气体。下图是他们实验中用过的仪器。请回答下列问题: 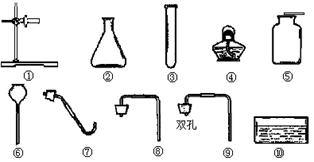 (1)小明同学在制取气体时使用的仪器是①③④⑤⑦⑩,他制取的气体是_____(填化学式); 制取该气体时发生反应的化学方程式是__________________________________。 (2)小敏同学顺利地制取并收集了一瓶二氧化碳,已知她已经使用了仪器②⑥,那么她还一定使用了上图仪器中的________________(填序号);制取二氧化碳的化学方程式是 _________________________________________________。 23. (5分)某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如右图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成。 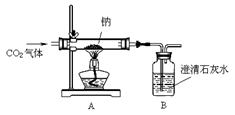 【资料卡】 【资料卡】(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱; (2)钠为银白色金属,过氧化钠(Na2O2)为淡黄色固体。 【提出问题】白色固体含有什么物质? 【猜想与假设】 假设1:白色固体是一种纯净物,仅含有____________; 假设2:白色固体是一种混合物,含有Na2CO3和Na2O; 【实验设计】
【反思提高】 Na在CO2中燃烧存在多个反应、生成多种物质。若假设1成立,请写出Na在CO2中燃烧的化学方程式:__________________________________。 四、计算题(本大题包括1小题,共7分。)  24.(7分)为了测定生铁中铁的质量分数,某校化学学习小组进行了实验研究,取6 g生铁与溶质的质量分数为10%的盐酸反应(生铁中杂质不溶于水,也不与盐酸、硫酸铜溶液反应),并绘制了加入盐酸质量与放出气体质量的关系图。 24.(7分)为了测定生铁中铁的质量分数,某校化学学习小组进行了实验研究,取6 g生铁与溶质的质量分数为10%的盐酸反应(生铁中杂质不溶于水,也不与盐酸、硫酸铜溶液反应),并绘制了加入盐酸质量与放出气体质量的关系图。(1)a=________。 (2)6 g生铁与溶质的质量分数为10%的盐酸恰好完全反应时所得不饱和溶液中溶质的质量分数为多少?(保留一位小数) (3)小华同学又设计了一个实验方案:另取6 g该生铁粉末与溶质的质量分数为20%的硫酸铜溶液反应来测定生铁中铁的质量分数。当加入80 g硫酸铜溶液时,所得固体的质量为______。 参考答案 1.C 2.B 3.A 4.B 5A 6.B 7.D 8.C 9.B 10.C 11.A 12.D 13.D 14.B 15.B 16. (1)2H (2)3Al3+ 17. (1) 挥发性 (2)见光或受热易分解 (3)密封、避光、阴凉处保存 18.(1)16 g (2)冷却热饱和溶液 (3)B、C、A 19. (1)H+、SO42-、H2O ;2NaOH+CuSO4===Cu(OH)2↓+Na2SO4 (2)3CO+Fe2O3  2Fe+3CO2 2Fe+3CO2 (3)C或H2 20. (1)镁片与稀盐酸反应比铁片与稀盐酸反应剧烈 (2)Cu+2A gNO3====Cu(NO3)2+2A g (3) Cu ,稀盐酸 21.(1)C、B、A (2) B、C 22. (1)O2 , 2KClO3 (2)⑤⑨ ,CaCO3+2HCl===CaCl2+CO2↑+H2O 23. 假设1:Na2CO3 【实验设计】
【反思提高】4Na+3CO2 24.(1)0.2 (2) 16.2% (3)6.8 g (责任编辑:admin) |
