|
☆☆☆ 点击下载试题 ☆☆☆ 2017年安徽省中考化学试题注意事项: 1.化学试卷共三大题16小题 2.试卷包括“答题卷”和“试题卷”两部分,试题卷共四页,答题卷共两页。 3.请务必在“答题卷”上答题,在“试题卷”上答题是无效的。 4.考试结束后请将“答题卷”和“试题卷一并交回”。 可能使用相对原子质量: H-1 He-4 O-16 Na-23 C1-35.5 K-39 一、2017年安徽省中考化学试题本大题包括10小题,每小题2分,共20分。每小题的四个选项中有一个符合题意。  1. 化学在生产生活中应用广泛,下列过程属于化学变化的是( ) A.海水晒烟 B.活性炭净水 C.煤制煤气 D.干冰降雨 2. “珍惜资源,保护环境”是每位公民应尽的义务,下列相关做法错误的是( A.我国稀土储量世界第一,可以任意开发利用 B.研发秸秆综合利用技术,避免因直接焚烧造成大气污染 C.利用二氧化碳捕捉技术,减少我国二氧化碳引起的“温室效应” D.改造城市 3. 在最新公布中文名称的元素,该元素相关信息如图所示。下列有说法正确的是( )  A. 元素符号为 uUO A. 元素符号为 uUO B. 原子序数为 118 C. 原子的质数为 176 D. 相对原子质量为 294g 4. 下列实验装置或操作正确的是( )  A.加热液体 B.加入固体 C.检查气密性 D、收集氧气 5. 生活习惯直接影响人体健康 ,小明同学一家人的下列饮食习惯科学合理的( ) A.小明长期偏食“洋快餐” B.奶不忍浪费,即使食物霉变仍然用 C.妈为了保持身材,只吃蔬菜和水果 D.爸享受运动,大量出汗后常饮用含无机盐的饮料 6. 建立模型是学习化的重要方法,下列有些正确( )  A.原子结构模型 B.物质分类模型 C.燃烧条件模型 D.空气组成模型 7. 据报道,我国科学家发现一种氦钠化合物(化学式为 Na2He)。下列说法正确的是( ) A. Na2He中Na为+1 价,He 为-1价 B. Na2He中Na、He元素质量比为 2:1 C. Na2He中既含金属元素,又含非金属元素 D.稀有气体很稳定,不与任何物质发生反应 [来源:学,科,网Z,X,X,K] 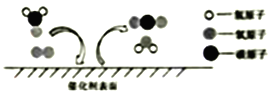 8. 科学家发现,利用催化剂可有效消除室内装修材料释放的甲醛,其反应微观 A.属于置换反应 B.可解决甲醛带来的室内空气污染问题 C.其中甲醛属于氧化物 D 9. 下列实验事实不能作为相应观点的证据是( )
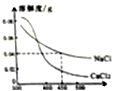 10. 地球深处的水处于超临界状态,称为超临界水。下图为某压强下CaCl2 和NaCl 在超临界水中的溶解度曲线,该压强下,下列说法正确是( ) 10. 地球深处的水处于超临界状态,称为超临界水。下图为某压强下CaCl2 和NaCl 在超临界水中的溶解度曲线,该压强下,下列说法正确是( )A.在超临界水中,NaCl的溶解度大于CaCl2的溶解度 B.在超临界水中,2种物质的溶解度都随温升高而增大 C. 450℃时,NaCl在超临界水的溶解度为 0.04g D.450℃时,可得到 0.04%的CaCl2的超临界水溶液 二、 2017年安徽省中考化学试题本大题包括 本大题包括 5小题,共 34 分 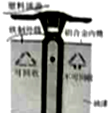 11. (6分)近年我省多地纷纷展开文明城市创建工作,垃圾分类回收是其中一项重要举措。某地街头垃桶如右图所示,回答下列问题。 11. (6分)近年我省多地纷纷展开文明城市创建工作,垃圾分类回收是其中一项重要举措。某地街头垃桶如右图所示,回答下列问题。(1)图中标识的物质,属于金属材料是 ________ (写出一种即可下同),属于有机合成材料的是__________。 (2)塑料矿泉水瓶应收入________(填“可回收”或“不可回收”)筒中。 (3)使用铝合金做内筒的优点是 (写出1点即可)。 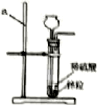 (4)为比较铝和铁的金属活动性,某同学设计实验方案:将铝和铁分别放入盐酸中,比较反应的剧烈程度。你认为该方案__________(填“合理”或“不合理”),理由是 (4)为比较铝和铁的金属活动性,某同学设计实验方案:将铝和铁分别放入盐酸中,比较反应的剧烈程度。你认为该方案__________(填“合理”或“不合理”),理由是 12.(6 分)实验室常用右图所示发生装置 (1) (2)仪器a 的名称是_________。实验室可用 方法收集氢气。 (3)氢气作为新能源的优点是 (写出1 点即可,下同)。目前氢能源的 大量使用仍存在一定困难,你认为针对氢能源的研究方向是 。 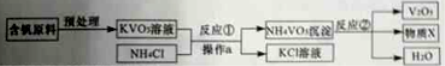 13.(7 分)五氧化二钒(V2 O5)是一种工业催化剂,下图是制取V2 O5 的工艺流程。 (1)写出反应①的化学方程式 。 (2)操作a 的名称是_________,实验室进行该操作所需的玻璃仪器有烧杯、玻璃棒和 。 (3)反应②的反应类型是 ,物质X一定含有的元素是__________。 (4)写出副产物KCl 的一种用途___________。 14.(7 分)某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸用下图装置完成表中实验,回答下列问题。
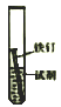 (1)铁锈的主要成分是__________(填化学式)。 (2)实验②和④可探究_________ 因素对铁制品锈蚀快慢的因素;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是________(填实验序号)。 (3)根据表中实验现象得出的结论是 (写出1 点即可)。 (4)影响铁制品锈蚀快慢受除上述因素外,还有 (写出1 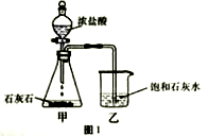 15.(8 分)某兴趣小组用图1 装置进行实验时发现,烧杯中饱和石灰水先变浑浊,后逐渐澄清。 (1)写出甲装置中发生反应的化学方程式 ;石灰水变浑浊是因为生成了 。(填化学式) (2)为探究“饱和石灰水浑浊后变澄清的原因”,该小组同学开展了如下活动: 【查阅文献】碳酸钙(碳酸钠等)与二氧化碳、水反应生成可溶于的碳 【提出假设】假设 1:挥发出的HCl使浑浊变澄清;  假设 2: 。 假设 2: 。【设计实验】为除去 CO2中的 HCl,小华 装置的连接顺序是甲→ → →乙(填字母序号);其中存放的试剂合理 是 (填选项序号)。 A. 浓硫酸 B.NaOH 溶液 C. 饱和Na2CO3溶液 D. 饱和NaHCO3溶液 【实验现象】饱和石灰水浑浊后,继续通入足量 CO2 ,沉淀部分溶解但最终并未完全澄清。 【得出结论】由以上探究可得出结论是 。 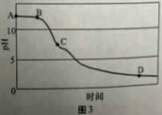 【注意:答对第(3)小题奖励 4分,化学试卷总不超过 60 分。】 【注意:答对第(3)小题奖励 4分,化学试卷总不超过 60 分。】(3)该兴趣小组在老师指导下,用 PH 传感器测得图 1烧杯中溶液的 PH 随通入时间的变化曲线如图3。 ①AB 段 PH 值不变的可能原因是 ; D点所得溶液的成分除 H2O外还有 。 ②BC 段发生的化学方程式主要有 三、本大题共 、本大题共 6分 16.(6分)实验室加热氯酸钾和二氧化碳的混合物28g制取氧气,完全反应后剩余固体质量为18.4g,请计算: (1)生成氧 (2)原混合物中氯酸钾的质量。 2017年安徽省中考化学试题参考答案 1-10:CABDD DCBAC 11:(1) 铝合金内筒( 或铁制外筒); 塑料顶盖; (2) 可回收; (3) 不易生锈; (4) 不合理;只有相同条件下才有可比性(比如铝表面有致密性氧化铝薄膜, 金属的质量核表面积不相等) 12:(1) Zn+H2SO4=H2↑+ZnSO4 (2) 铁架台;向下排空气法( 或排水法); (3) 氢气燃烧产物是水,不污染环境;电解水 13.(1) KVO3+NH4Cl=NH4VO3 (沉淀)+KCl; (2) 过滤,漏斗 (3) 分解反应; (4) 制备钾盐 14.(1) 三氧化二铁( Fe2O3); (2) 温度; ①②或③④ (3) 相同条件下,酸性越强,金属生锈越快; (4) 酸的浓度,相同条件下, 取两份不同浓度的醋酸分别在 25 摄氏度下观察铁钉的生锈时间 15.(1) 2HCl + CaCO3 = CaCl2 + CO2 ↑+ H2O; CaCO3; (2)【提出假设】 生成的 CO2 使混浊变澄清; 【设计实验】 b , a ; D 【得出结论】 假设 2 成立: 通入 CO2, CaCO3 会进一步与 CO2 和 H2O 发生反应, 生成 Ca(HCO3)2(不是沉淀) (3)附加题: ①一开始排出来的是空气,不与 CaCO3 反应变成 Ca(HCO3)2; HCl ②Ca(OH)2+CO2=CaCO3(沉淀)+H2O 三、 16.(1) 生成氧气的质量 m(O2)=28.0g-18.4g=9.6g (2)设氯化钾的质量为 Xg. 2KClO3 = 2KCl + 3O2(气体) 245 96 X 9.6g 解得:X=24.5g (责任编辑:admin) |
