|
2008年连云港市中考化学模拟试题 连云港赣马二中 赵中明 一、选择题(每题2分,共40分,每小题只有一项最符合题目要求) 1.下列物质中,属于纯净物的是  2. 在日常生活中,如果将深颜色的衣服和浅颜色的衣服浸泡在一起,可能会使浅色衣服染上深颜色,这其中的主要原因是由于深色染料中的 A.分子本身发生了改变 B.分子是在不断地运动的 C.分子间的间隔增大 D.分子在化学变化中可分 3. 2007年10月24日,我国使用“长征三号甲”运载火箭将“嫦娥1号”送上月球轨道,其任务之一是探测月球上氦–3(质子数为2,中子数为1的原子)资源。下列氦–3原子的原子结构示意图中正确的是 4.“以崇尚科学为荣,以愚昧无知为耻”。下列叙述缺乏科学依据的是 A.不可用工业酒精勾兑饮用酒 B.小孩经常咬铅笔芯,会导致铅中毒 C.加碘食盐的“碘”是指碘元素 D.用纯碱可除去面团发酵产生的酸 5. 下列各组物质的名称、俗称、化学式表示同一物质的是 A.氢氧化钠 纯碱 Na2CO3 B.氯化钠 食盐 NaCl C.硫酸铜晶体 胆矾 CuSO4 D.碳酸钙 生石灰 Ca(OH)2 6. 下列实验方案中,可行的是 A. 按溶解、过滤、蒸发的操作顺序可以分离CaCl2、CaCO3的混合物 B. 向某种溶液中加入氯化钡溶液,产生白色沉淀,证明该溶液一定是硫酸 C. 用磷在密闭容器中燃烧,除去密闭容器内空气中的氧气 D. 用玻璃棒蘸取食用白醋滴在润湿pH试纸上,测定其pH 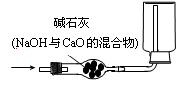 7. 以下是我们熟悉的几种气体,其中可用右图所示装置干燥并收集的是(省略了铁架台等仪器) 7. 以下是我们熟悉的几种气体,其中可用右图所示装置干燥并收集的是(省略了铁架台等仪器)①H2 ②O2 ③CO2 ④SO2 ⑤CH4 A.①② B.③④ C.①⑤ D.①②⑤ 8. 水冷却后,除了会凝固成冰晶体外,还会形成玻璃态。它是由液态水急速冷却到-1 080C时形成的,玻璃态的水与普通液态水的密度相同。下列说法正确的是 A.水由液态变为玻璃态,体积减小 B.水由液态变为玻璃态,体积膨胀 C.水由液态变为玻璃态是物理变化 D.水由液态变为玻璃态是化学变化 9. 我省巢湖市的温泉远近闻名。分析鉴定可知,该地区温泉的水中含有较多的硫酸根离子,以及钾、钠、钙、锌、锶等多种对人体有益的微量元素。下列关于硫酸根离子的鉴定方法中,正确的是 A.滴加盐酸 B.滴加Ba(NO3)2溶液后,再加稀HNO3 C.滴加NaOH溶液后,再加稀盐酸 D.加Na2CO3溶液后,再加稀HNO3 10. 把一杯饱和NaCl溶液加热蒸发掉一些水分后,冷却至原来的温度,保持不变的是 A.溶液的质量 B.溶质的质量分数 C.溶液中溶质的质量 D.溶剂的质量 11.新华网3月14日报道,我国首先在世界上实现了二氧化碳聚合物大规模工业化生产。 二氧化碳聚合物是二氧化碳在催化作用下,生成的高分子化合物。它具有良好的阻气性、透明性和使用后全降解无污染等优点,广泛用于医药和食品包装、一次性餐具等行业。下列有关二氧化碳聚合物的说法,错误的是 A.二氧化碳聚合物的生产和使用,可有效的防止其它塑料产生的白色污染 B.二氧化碳聚合物生产原料为二氧化碳,原料非常丰富且价格低廉 C.二氧化碳聚合物是二氧化碳的固体 D.二氧化碳聚合物的生产和使用,既减少了温室气体二氧化碳的排放,又得到了非常有用的产品,真正做到了“变废为宝” 12.下列各组固体物质,只用水不能进行鉴别的是 A.CaCO3、Na2CO3 B.K2SO4、KCl C.生石灰、熟石灰 D.CuSO4、Fe2(SO4)3 13.实验室中装有浓硫酸的试剂瓶应贴有的图标是  A B C D 14.我们中华民族的祖先在世界冶金史上曾谱写过辉煌的篇章。早在距今2000余年前的西汉时期,就有“曾青得铁则化为铜”的记述,此乃现代湿法冶金术之先驱。从现代化学观点理解,“曾青”应赋予的最恰当涵义为 A.铜(单质) B.硫酸铜(溶液) C.铜的化合物 D.可溶性铜盐(溶液) 15.类推是一种重要的学习方法,但如果不具体问题具体分析就会产生错误的结论。下列类推结论正确的是 A.原子在化学变化中不能再分,则分子在化学变化变化中不能再分 B.KNO3溶于水时溶液温度无明显变化,则NH4NO3溶于水时溶液温度也无明显变化 C.点燃H2与O2混合气体可能爆炸,则点燃CH4与O2 的混合气体也可能爆炸 D.CuO不能与水反应,则CaO也不能与水反应 16.向盛有4.9g20%的硫酸中,慢慢滴加10g20%的Ba(OH)2溶液,能正确表示其变化图像是 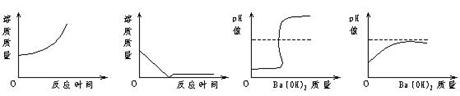 A B C D 17.在水溶液中,一般不会与其它物质发生复分解反应的是 A.NaCl B.KNO3 C.NaOH D.H2SO4 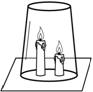 18. 如图,将两支燃着的蜡烛罩上茶杯,一会儿后高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从着火燃烧的高层房间中逃离,下列方法中正确的是 18. 如图,将两支燃着的蜡烛罩上茶杯,一会儿后高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从着火燃烧的高层房间中逃离,下列方法中正确的是 A.用湿毛巾捂住鼻子 B.成站立姿势跑出 C.沿墙角直立身子迅速爬向门外 D.打开窗户跳出 19. 今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-。现取两份200 mL溶液进行如下实验:① 第一份加足量NaOH溶液,加热,收集到气体0.68 g;② 第二份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是 A.一定不存在Ba2+,NH4+可能存在 B.CO32-一定存在 C.Na+一定不存在 D.一定不存在Cl- 20. 下列图象关系正确的是 A.表示CO还原CuO的实验中,试管内的固体质量与反应时间的关系图 B.表示向一定量的稀硫酸中加入过量Ba(OH)2溶液,溶液的pH与Ba(OH)2溶液体积的关系图 C.表示一定温度下,向一定量的饱和氯化钠溶液中不断加入蔗糖晶体时,溶液的质量与蔗糖质量的关系图 D.表示向足量的稀CuCl2中加入少量Fe,溶液质量与时间的关系图 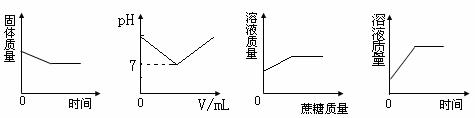 A B C D 二、填空题(本题包括3小题,共24分) 21.(11分)从Ca、C 、 S 、H 、O 、N六种元素中选择适当的元素或由其组成的物质,按要求完成下列各题。 (1)写出符合下列要求的化学符号: ①二个氢分子 ; ②三个硫酸根离子 ; (2)写出符合下列要求的物质的化学式: (3)写出符合下列要求的化学方程式: ①用石灰石制生石灰分解反应 ; ②有水生成的化合反应 ; ③稀硫酸与熟石灰发生的中和反应 。
(1)写出固体混合物与盐酸发生化学反应的化学方程式: 、 。 (2)试通过分析计算出混合物中Na2CO3的质量分数为多少? 2008年中考化学模拟试题 参考答案
二、(本题包括3小题,共24分) 21、(11分) (1)①2H2 ② 3SO42- (2) ①CH4 ②CaO ③H2O ④C ⑤CaCO3 ⑥H2SO4 (3)①CaCO3高温CaO+CO2↑ ②2H2+O2点燃2H2O ③Ca(OH) 2+H2SO4=CaSO4+2H2O(方程式没有配平的每个扣0.5分,缺少条件的每个扣0.5分,扣分不超过1分) 22、(7分)(每空1分) (1)A; (2)能使用外焰加热; (3)糖类 C (4)使可燃物与空气(或氧气)充分接触; (5)C (6)AB 23、(6分)(每空1分) (1)②⑧⑨⑩(少两个或三个扣0.5分,少一个不扣分,多一个扣1分) (2)SO2+Ca(OH) 2=CaSO3+H2O (3)利用太阳能使水分解制取氢气 产物是水不污染环境(或:无污染); (4)化学能 Li 或Li和Mn 三、(本题包括3小题,共19分) 24.(1)① (2)CaCO3 水 300 能量 25.(7分) ⑴(4分)Fe2O3 CaCO3 C CuSO4 (或CuCl2) (2)(6分)FeCl3+3NaOH=Fe(OH)3↓+3NaCl (2分) Fe2O3+3CO 高温 2Fe+3CO2 (2分) Fe+ CuSO4=FeSO4+Cu或Fe+ CuCl2=Fe Cl2+Cu (2分) 26.(每空一分,共7分) 氮肥 ; Ca(OH)2 、酸性; 熟石灰的反应; 氨气的水溶液呈碱性,如有氨气释放出来的话,则PH试纸变色; 避免与碱性物质共存(其它合理答案均得分) 四、(本题包括1小题,共11分) 27(11分) (1) 反应物的状态和反应条件等 图2 (2) 漏斗颈中形成一段稳定的水柱(或液面不再下降)等 (3) ①吸收二氧化碳中混有的氯化氢气体 NaHCO3+HCl==NaCl+H2O+CO2↑ ②干燥二氧化碳 浓硫酸 (4)将带火星的木条放在集气瓶上方的导管口附近 (5)C装置处的澄清石灰水变浑浊 (6)2Na2O2+2H2O===4NaOH+O2↑ (7)35.1kg。 五、(本题包括1小题,共6分) 28.(6分)【数据处理】从图中得知:产生CO2的最大量为2.2g。 (1)解:设该样品中Na2CO3的质量为x,则: Na2CO3+H2SO4==Na2SO4+H2O+CO2↑…………………………………………(1分) 106 44 x 2.2g ……………………………………………(1分) (2)则样品中NaOH质量分数为: 答:样品中Na2CO3的质量为5.3g;NaOH的质量分数为75.0%。 【反思与交流】①NaOH ②相同 …………………………………………(2分) 29.(1)丙(1分) (2)NaOH+HCl==NaCl+H2O(1分) Na2CO3+2HCl==2NaCl+H2O+CO2↑(1分) (3) CO2的质量=141.20g+10.0g-149.0g=2.2g ( 1分 ) 解:设原混合物中Na2CO3的质量为x。 ……………… ( 0.5分 ) Na2CO3 + 2HCl = 2NaCl + H2O + CO2 ↑ 106 44 x 2.2 g 混合物中Na2CO3的质量分数为(5.3g÷10.0g)×100%=53.0% ………………(1分) 答: 混合物中Na2CO3的质量分数为53.0%.……………… 0.5分 (责任编辑:admin) |

 三、填空题(本题包括3小题,共19分)
三、填空题(本题包括3小题,共19分)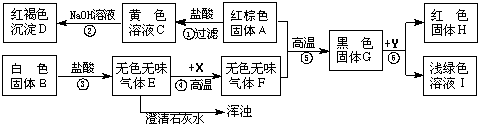
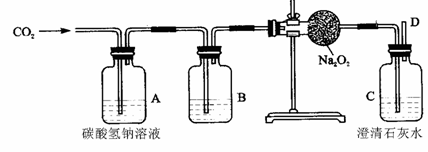
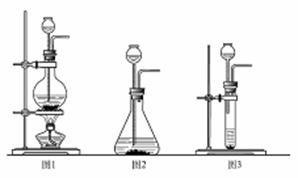
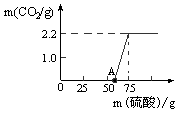 【设计方案】先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数。
【设计方案】先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3的质量,从而进一步确定样品中NaOH的质量分数。 称 量 项 目
称 量 项 目