|
北京市海淀区2010—2011学年度第一学期初中化学期末试卷 北京 李菁菁(供稿)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Cl 35.5 K 39 Ca 40 一、选择题(每小题只有1个选项符合题意,共25个小题,每小题1分,共25分。) 1. “低碳生活”是指生活作息时所耗用的能量要尽量少,减低二氧化碳排放量,保护环境。下列做法符合“低碳生活”理念的是
 2.下列关于“白色污染”(见右图)的说法,不正确的是 2.下列关于“白色污染”(见右图)的说法,不正确的是A.“白色污染”破坏土壤,污染地下水 B.“白色污染”是指白色的垃圾造成的污染 C.用布袋代替塑料袋可以减少“白色污染” D.使用一些新型的、可降解的塑料可以减少“白色污染” 3.下列变化中,属于化学变化的是
4.下列关于空气的说法,正确的是 A.空气中只有单质 B.空气是一种纯净物 C.空气是一种重要的资源 D.空气中氧气的质量分数为21% 5.汽车碰撞后安全气囊中迅速发生化学反应,生成一种空气中含量最多的气体,该气体是
6.能使带火星木条复燃的气体是
7.自然界的水常常遭到人为污染。例如使用含磷洗衣粉的生活污水会造成水中藻类大量繁殖,使水质恶化。这里的“磷”是指
8.生活离不开水。下列各种水中,纯度最高的是
9.下列关于仪器用途的叙述,不正确的是 A.试管用作反应容器 B.量筒用作反应容器 C.玻璃棒用来过滤时引流 D.托盘天平用来称量物质质量 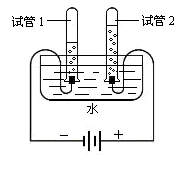 10.下列关于右图所示实验的说法,正确的是 10.下列关于右图所示实验的说法,正确的是A.该反应为化合反应 B.试管1中的气体是氢气 C.试管1和试管2中气体体积比为1:2 D.该实验证明水是由氢气和氧气组成的 11.人们从长期的生产实践中逐步认识到,物质是由各种微观粒子构成的。下面事实能说明粒子在不停运动的是
12.根据化学实验常识,判断下列事故处理方法正确的是 A.炒菜时油锅着火,立即盖上锅盖 B.家用电器着火时,立即用水浇灭 C.高层住房着火时,立即打开所有门窗 D.发现煤气泄露时,立即打开排风扇电源开关 13.潜艇中船员呼吸产生的二氧化碳能通过化学反应2 Na2O2 + 2CO2 = 2X + O2吸收,则X的化学式为
14.下图所示的实验操作,正确的是 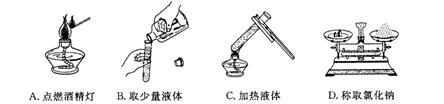 15.实验室用高锰酸钾制氧气,实验结束前需要进行的操作是 A.先把试管取下,再熄灭酒精灯 B.先熄灭酒精灯,再把导管从水槽中取出 C.先把导管从水槽中取出,再熄灭酒精灯 D.先熄灭酒精灯,再把试管取下,最后把导管从水槽中取出  16.“海宝”是2010年上海世博会的吉祥物。某“海宝”玩具的外用材料为纯羊毛,内充物为聚酯纤维。区别这两种物质的最好方法是 16.“海宝”是2010年上海世博会的吉祥物。某“海宝”玩具的外用材料为纯羊毛,内充物为聚酯纤维。区别这两种物质的最好方法是
17. 下图所示实验中,紫色小花变红的是  ①喷稀醋酸 ②喷水 ③直接放入二氧化碳中 ④喷水后放入二氧化碳中
18.向充满CO2的软塑料瓶倒入适量澄清的石灰水后,迅速拧紧软塑料瓶的瓶盖并振荡,实验现象有:①澄清的石灰水变浑浊 ②软塑料瓶变瘪并发出声音 ③塑料瓶内液体由紫色变红 ④塑料瓶内液体变得烫手
 19. 根据右图所示实验,不能得到的结论是 19. 根据右图所示实验,不能得到的结论是A.CO2不能燃烧 B.CO2不支持燃烧 C.CO2密度比空气大 D.蜡烛燃烧生成CO2和H2O 20.乙酸(CH3COOH)是食醋的有效成分。下列关于乙酸的说法,正确的是 A.乙酸由4种元素组成 B.一个乙酸分子中含有8个原子 C.乙酸分子的相对分子质量为60 g D.乙酸分子中碳元素与氧元素的质量比4:3 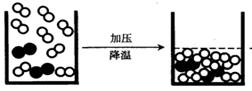 21.下列关于右图的说法中,正确的是 21.下列关于右图的说法中,正确的是A.装置内为纯净物 B.该变化是物理变化 C.该变化是化合反应 D.本实验说明分子间没有空隙 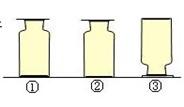 22.右图是放置在实验桌上的三瓶无色气体,它们分别是H2、O2、CO2中的一种。下列关于这三种气体的说法中,正确的是 22.右图是放置在实验桌上的三瓶无色气体,它们分别是H2、O2、CO2中的一种。下列关于这三种气体的说法中,正确的是A.根据集气瓶的放置方法判断,瓶①②存放的是H2、CO2 B.用点燃的木条伸入②中,若火焰熄灭,则存放的是CO2 C.向②中加入少量蒸馏水,若变为红色,则存放的是CO2 D.用点燃的木条放入③中,若气体燃烧,则存放的是O2 23.下表各组中,实验操作和目的对应关系不正确的是
24.“绿色化学”能实现零排放(即反应物中的原子都转变为生成物)。CO和H2在一定条件下按照不同的比例可以合成不同的有机化工原料。根据零排放的要求,以CO和H2合成的有机物不可能是
25.为解决日益加剧的温室效应等问题,科学家正在研究建立如下图所示的二氧化碳新循环体系: 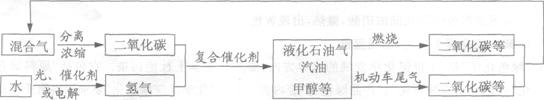 上述关系图能反映的化学观点或化学思想有: ①化学变化中元素种类是守恒的;②燃烧时化学能可以转化为热能和光能;③光能或电能可以转化为化学能;④无机物和有机物可以相互转化;⑤二氧化碳也是一种重要的资源。
二、填空题(共5个小题,共29分。) 26.(6分)第16届亚运会刚刚在广州闭幕,精彩的盛会给世人留下了深刻的印象。 (1)亚运会是科技的盛会。 ①广州亚运会使用了一种电能、太阳能混合动力电动车,用车顶的太阳能板把太阳能转化为电能。太阳能板中大量使用硅,该元素的种类属于 元素。 ②下列应用中,主要使用有机合成材料的是(填序号,下同) 。  (2)科学的饮食可以保证每一个与会者的健康。 ①运动员能品尝到虾饺等具有岭南特色的茶点。制作虾饺的主料有虾仁、冬笋、猪肉、面粉等,其中提供能量的营养素有蛋白质、 、油脂。 ②运动员需要多食用蔬菜、水果,补充各种维生素。缺乏维生素C会引起的疾病是(填序号) 。 a.坏血病 b.龋齿 c.夜盲症 ③人体健康离不开钙元素。下列有关钙元素的叙述中,不正确的是 。 a.幼儿及青少年缺钙会得佝偻病和发育不良 b.成年人比幼儿和青少年需要摄入更多的钙 c.老年人缺钙会发生骨质疏松,容易骨折 d.人体中钙元素大部分存在于骨骼和牙齿中 (3)广州亚运会是绿色亚运,据报道广州亚运的垃圾100%实现了分类处理和回收。请举出一种可以回收的垃圾: 。 27.(6分)能源、环境问题是全球关注的热点问题。 (1)生活中经常使用的燃料有煤、 和天然气等化石燃料。 (2)化石燃料大量使用产生 、NO2等污染物,这些污染物在空气中反应后的生成物溶于雨水,会形成 ,破坏环境。 (3)现阶段,人们大量利用燃料燃烧产生的能量。某校化学小组在研究燃烧的条件时,做了下图所示A、B、C三个实验。 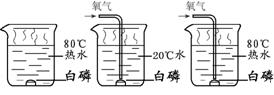 A. B. C. ①白磷能够燃烧的是实验是(填序号) , 反应的化学方程式为 。 ②对比实验B和C可以得到的结论是 。 28.(7分)氢气、氧气、二氧化碳和一氧化碳是初中化学中的常见物质,下图是它们的一些具体应用。  这些物质中: (1)可作制冷剂,用于人工降雨的物质是(填物质名称或化学式,下同) 。 (2)可以用于制作碳酸饮料的物质是 ,其中发生的化学方程式为 。 (3)高炉炼铁中一氧化碳还原氧化铁的化学方程式为 。 (4)可用作燃料的物质是 ,其燃烧的化学方程式为 。 29.(5分)物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙合成丙。甲、乙、丙的微观示意图见下表。 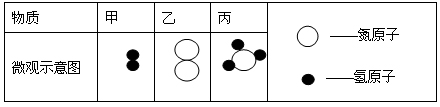 (1)甲、乙、丙三种物质都是由(填“分子”、“原子”或“离子”) 构成的。 (2)甲、乙、丙中属于化合物的是(填序号) 。 (3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 。 (4)甲和乙合成丙的反应中,甲、乙、丙的微粒个数比为 。 (5)现有10 g 的甲和60 g 的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4 g,则剩余乙的质量为 g。 30.(5分)化学实验小组同学对某小区下水管道中的气体样品进行研究。 已知:①下水管道气体中常含有二氧化碳、甲烷、氧气、氮气、硫化氢(H2S)等成分。 ②硫化氢是一种无色、有臭鸡蛋气味的气体。H2S通入CuSO4溶液中,反应生成CuS沉淀和硫酸(H2SO4),从而除去H2S。该反应的化学方程式为 。 (1)该下水管道中的气体有特殊臭味,气体中一定含有的气体是 。将该下水管道中的气体通过CuSO4溶液。 (2)将步骤(1)处理过的气体通入澄清石灰水中,澄清石灰水变浑浊,说明该下水管道中的气体含有二氧化碳。该反应的化学方程式为 。 (3)收集1小试管经过步骤(1)处理过的气体,移近酒精灯火焰,听到尖锐的爆鸣声,说明该下水管道中的气体还含有的气体是 。该反应的化学方程式为 。 三、实验题(共3个小题,共20分。) 31.(6分)根据下图回答问题。 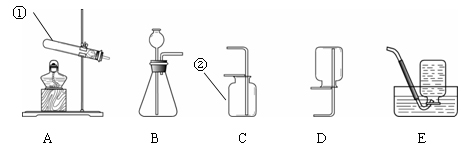 (1)写出标有序号的仪器名称:① ;② 。 (2)用高锰酸钾制取氧气时,所选用的发生装置是(填序号,下同) ,收集装置是C或 ,反应的化学方程式为 。 (3)用大理石和稀盐酸制取二氧化碳时,所选用的发生和收集装置为 。 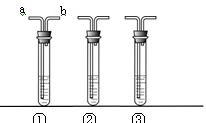 32.(6分)某实验小组探究火锅烟气中CO2、CO分别对人体血液供氧能力的影响。设计装置如图所示(试管中均为稀释的新鲜鸡血) 32.(6分)某实验小组探究火锅烟气中CO2、CO分别对人体血液供氧能力的影响。设计装置如图所示(试管中均为稀释的新鲜鸡血)实验记录:
(1)向试管①中通入气体时,气体从导管口(填装置图中的序号) 处通入。 (2)试管②的作用是 。 (3)气体A为 。判断的依据是 。 (4)从安全和环保的角度来看,本实验需要改进的地方是 。 (5)通过实验可以得出结论,火锅烟气中对人体血液供氧量有影响的是(填具体物质) 。 33.(8分)碳酸钙可用于预防和治疗钙缺乏症。某实验小组同学要测定一种钙片中碳酸钙的含量。 【查阅资料】获得的资料有: (1)补钙剂中常加入糖类、维生素D等改善口感或增强药效。这些物质不与稀盐酸反应产生气体,高温灼烧时会燃烧或分解。 (2)碳酸钙高温灼烧分解生成氧化钙和二氧化碳。 (3)常见的碳酸钙含量测定方法:将碳酸钙粉碎,加入已知浓度的过量盐酸充分反应,然后测剩余盐酸的量,根据消耗盐酸的量最终求得碳酸钙的含量。 (4)澄清石灰水中的Ca(OH)2含量很少,100 g澄清石灰水中最多含0.15 g Ca(OH)2。 【方案设计和实施】根据资料和已学知识,该小组同学设计如下两种方案进行测定。 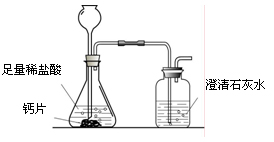 方案1:根据右图所示装置实验。 方案1:根据右图所示装置实验。(1)锥形瓶中发生反应的化学方程式为 。 (2)长颈漏斗下部插入液面下的目的是 。 (3)加入药品前,检验该装置气密性的方法是 。 (4)记录数据如下:
方案2:将钙片粉碎,加入足量的稀盐酸充分反应,根据放出气体的量计算碳酸钙的含量。记录数据如下(空烧杯质量为100 g,加入钙片质量为25 g):
【分析和评价】 (1)方案1和方案2中合理的是 ,原因是 。 (2)该小组同学没有使用碳酸钙高温灼烧分解的方法(实验室可以进行该实验),原因是 。 (3)要使用【查阅资料】(3)中介绍的方法,还需要学习的是 。 【结论】经过计算,该钙片中碳酸钙的质量分数是 。 四、计算题(共2个小题,共6分。) 34.(3分)铝是目前广泛使用的金属。工业上用电解氧化铝制取金属铝,反应的化学方程式为:2Al2O3  4Al + 3O2↑。如果加工一个铝锅需要1.08 Kg的铝,至少需要电解多少质量的氧化铝才能制成这个铝锅? 4Al + 3O2↑。如果加工一个铝锅需要1.08 Kg的铝,至少需要电解多少质量的氧化铝才能制成这个铝锅?35.(3分)急性腹泻会造成人体脱水,此时可服用补液盐补充水分。  某种口服补液盐的成分和用量如下。 某种口服补液盐的成分和用量如下。【成分】每包含葡萄糖11 g、NaCl 1.755 g、KCl 0.745 g、NaHCO3 1.260 g。 【用量】临用时,将一袋补液盐溶于500 mL温水中,一般每日服用3000 mL。 (1)补液盐中对维持人体内的水分和体液恒定的pH有重要作用的是 。 (2)按照说明书中一天的用量,由该补液盐补充的钾元素质量是 g。 (3)若在家中按照该补液盐中钾元素和钠元素的质量比,临时配制1包补液盐。如果钠元素全部由NaCl来提供,则需要用(写计算式即可) g NaCl来代替原配方中的NaHCO3。 海淀区九年级第一学期期末练习 化学试卷参考答案及评分标准 2011.1 一、选择题(每小题只有1个选项符合题意,共25个小题,每小题1分,共25分。)
说明:以下各问答案合理均给分,但不得超过题目规定的分数。简答题学生若多答其他内容,所答内容若正确不扣分,所答内容若不正确则扣分。 二、填空题(共5个小题,共29分。) 26.(共6分) (1)①非金属 ②c ……………………………………………………2分 (2)①糖类 ②a ③b ……………………………………………………3分 (3)空饮料瓶等合理即给分 ……………………………………………………1分 27.(共6分) (1)石油 ……………………………………………………1分 (2)SO2(写名称给分) 酸雨 …………………………………………2分 (3)①C 4P + 5O2  2P2O5 (写加热、不写条件不给分,下同) ……………2分 2P2O5 (写加热、不写条件不给分,下同) ……………2分②可燃物必须达到着火点才能燃烧(围绕控制着火点的意思说的都给分,单说控制温度不给分)…1分 28.(共7分) (1)干冰(或CO2) ……………………………………………………1分 (2)CO2 CO2 + H2O == H2CO3 ………………………………………………2分 (3)3CO + Fe2O3  2Fe + 3CO2 (高温、加热都给分) ……………………2分 2Fe + 3CO2 (高温、加热都给分) ……………………2分(4)CO、H2 (缺一不给分) 2CO + O2  2CO2 2H2 + O2 2CO2 2H2 + O2  2H2O ……………………2分 2H2O ……………………2分29.(共5分) (1)分子 ……………………………………………………1分 (2)丙 ……………………………………………………1分 (3)-3 ……………………………………………………1分 (4)3:1:2 ……………………………………………………1分 (5)32 ……………………………………………………1分 30.(共5分) ②H2S + CuSO4 == CuS↓ + H2SO4 ……………………………………1分 (1)H2S ……………………………………1分 (2)CO2 + Ca(OH)2 === CaCO3↓ + H2O ……………………………………1分 (3)CH4、O2(缺一不给分) ……………………………………1分 CH4 + 2O2  CO2 + 2H2O ……………………………………1分 CO2 + 2H2O ……………………………………1分三、实验题(共3个小题,共20分。) 31.(共6分) (1)①试管 ②集气瓶 ………………………………2分 (2)A E 2KMnO4  K2MnO4 + MnO2 + O2↑ …………3分 K2MnO4 + MnO2 + O2↑ …………3分(3)BC ……………………………………………………1分 32.(共6分) (1)a ……………………………………………………1分 (2)作对照实验(答出对比的意思就给分) ………………………………1分 (3)CO ……………………………………………………1分 通入A后鸡血颜色由鲜红色变为桃红色,再通入氧气,鸡血颜色不变的现象说明气体A使血红蛋白(血液)不能很好的与氧气结合,体现CO的毒性(建议同时答出现象和结论;结论答气体A影响血液供氧能力给分) ……………………1分 (4)增加CO尾气处理装置(不答CO不给分;答剩余CO直接排放、未处理等给分)………1分 (5)CO2和CO ……………………………………………………1分 33.(8分) 【方案设计和实施】 (1)CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ ………………………………1分 (2)防止CO2气体逸出(液封) ……………………………………………1分 (3)夹住胶管(堵住导管出口),从长颈漏斗加水至长颈漏斗中液面高于锥形瓶内液面,若一段时间不下降,则证明该装置气密性良好(必须答出操作、现象和结论才给分;答“先将长颈漏斗下部液封,将出口导管置于液面下,加热锥形瓶或用手捂住锥形瓶,有气泡产生,则证明该装置气密性良好”也给分)…1分 【分析和评价】 (1)方案2 ……………………………………………………1分 澄清石灰水中的Ca(OH)2含量很少(不足),吸收的二氧化碳量很少(建议答出因果关系)…………1分 (2)加入的糖类、维生素D等物质高温灼烧时会燃烧或分解,导致最终的数据偏大(建议答出因果关系)……1分 (3)如何测定未知浓度(剩余)盐酸的量 ……………………………………1分 【结论】60% ……………………………………1分 四、计算题(共2个小题,共6分。) 34.(3分)解:设需要电解的氧化铝质量为x 2Al2O3  4Al + 3O2↑ 4Al + 3O2↑ 204 108 x 1.08 Kg ……………………………………1分 x = 答:需要电解的氧化铝质量为2.04 Kg。 35.(3分) (1)钠、钾(答元素、离子均给分;答全物质也给分) ………………………1分 (2)2.34 …………………………………………………………1分 (3)58.5×0.015 或 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
