|
2012年湖北鄂州市初中毕业生学业考试模拟演练化学试题 姜菊梅 杨国安 相对原子质量:H—1 C—12 O—16 Cl—35.5 Na—23 一、选择题(本大题包括10小题,每小题只有1个选项符合题意。每小题2分,共20分) 1.日常生活中的下列现象,属于化学变化的是 ( ) A.湿衣服晾晒后变干 B.牛奶变酸 C.冰雪融化 D.轮胎爆裂 2.将深色的衣服和浅色的衣服浸泡在一起,会使浅色衣服染上深颜色,其中的主要原因是深色染料的 ( ) A.分子在不断地运动 B.原子本身发生变化 C.分子间的间隔增大 D.原子在化学变化中可分 3.金属钒被誉为“合金的维生素”。五氧化二钒(V2O5)中钒元素的化合价为( ) A.-3 B.+1 C.+3 D.+5 4.已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32,如果该氧原子的质量为m,则该硫原子的质量为 ( ) A.32m B.2m C.m D.不能确定 5.分类法是化学学习和研究的主要方法之一,下列分类正确的是 ( ) A.非金属元素:Mg、F、Si B.盐:纯碱、小苏打、硫酸铝 C.混合物:空气、石油、冰水混合物 D.合成材料:塑料、羊毛、合金 6.镁能在二氧化碳中燃烧:2Mg+CO2 A.Mg B.CO2 C.MgO D.C 7.向AgNO3、Cu(NO3)2、Mg(NO3)2的混合液中加入一些铁粉,待完全反应后,再过滤。下列情况不可能存在的是( ) A.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+、Mg2+ B.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+、Mg2+ C.滤纸上有Ag、Cu,滤液中有Fe2+、Mg2+ D.滤纸上有Ag、Cu、Fe,滤液中有Fe2+、Mg2+ 8.如图是A、B、C三种固体物质的溶解度曲线图,下列说法错误的是 ( ) 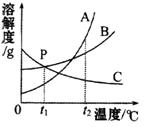 A.t2℃时,A、B、C三种物质中,A物质的溶解度最大 A.t2℃时,A、B、C三种物质中,A物质的溶解度最大B.P点表示t1℃时B、C两物质的溶解度大小相等 C.一定温度时,要将B物质的不饱和溶液转变成饱和溶液,可采取增加溶质的方法 D.20℃时,给A、B、C三种物质的饱和溶液加热(不考虑溶剂的蒸发),有晶体析出的是A物质 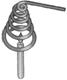 9.某同学在研究物质燃烧的条件时,做了如图所示的实验:把一条粗金属丝绕成线圈罩在一支蜡烛的火焰上,火焰很快就熄灭了。对这一实验的说法不正确的是( ) 9.某同学在研究物质燃烧的条件时,做了如图所示的实验:把一条粗金属丝绕成线圈罩在一支蜡烛的火焰上,火焰很快就熄灭了。对这一实验的说法不正确的是( )A.金属线圈内的气体温度升高了 B.可燃物的温度降到了着火点以下 C.金属丝有良好的导热性 D.若预先将金属丝加热,蜡烛就不会很快熄灭 10.下表是某同学整理的实验报告,其中错误的是 ( )
二、填空题(本大题包括2小题,每空2分,共12分)
三、实验题(本大题包括2小题,每空2分,共12分)
⑵是否需要做“向Fe2O3中加入水”的对比实验?为什么? 。 ⑶写出盐酸清除铁锈的化学方程式: 。
四、计算题(本大题只有1小题,6分) 15.将11g含少量杂质(杂质不溶于水,也不溶于酸)的碳酸钠固体,加入到43.8g盐酸中,恰好完全反应,产生二氧化碳气体4.4g。计算: ⑴原固体中碳酸钠的质量。⑵反应后的溶液中氯化钠的质量分数。 鄂州市2012年初中毕业生学业考试模拟演练化学试题参考答案及评分标准 二、填空题(本大题包括2小题,每空2分,共12分) 12.⑴CuCl2 ⑵CuCl2+Ba(OH)2=== BaCl2+ Cu(OH)2↓ ⑶复分解反应 三、实验题(本大题包括2小题,每空2分,共12分) 四、计算题(本大题只有1小题,6分) |

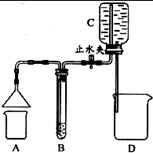 13.化学兴趣小组用如图所示装置(夹持仪器已略去)做了2个兴趣实验,每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡冒出。回答下列问题。
13.化学兴趣小组用如图所示装置(夹持仪器已略去)做了2个兴趣实验,每次实验时,打开止水夹,均可见C瓶内的水流入D中,B中有气泡冒出。回答下列问题。