|
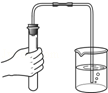
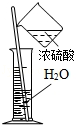
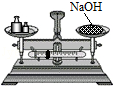
☆☆☆ 点击下载试题 ☆☆☆ 各位同学在查看时请点击全屏查看 2018年黔东南中考化学复习题 本试卷分卷I和卷II两部分。卷I为选择题,卷II为非选择题。 本试卷总分120分,考试时间为120分钟。 以下数据可供解题时参考: 相对原子质量: H-1 O-16 C-12 Mg-24 Cl-35.5 Na-23 Ag-108 卷I(选择题,共44分) 注意事项:1.答卷I前,考生务必将自己的姓名、准考证号、科目填涂在答题卡上。考试结束,监考人员将试卷Ⅱ和答题卡一并收回。(卷I由学生自己保管) 2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。答在试卷上无效。 一、选择题(本大题共22个小题;每小题2分,共44分。在每小题给出的四个选项中,只有一个选项符合题意) 1.以下特产制作的部分过程中涉及到化学变化的是( ) A.生产红糖时蒸发甘蔗汁液 B.酿制红曲酒时发酵糯米 C.制作火腿时将成品切块包装 D.制作蜜枣时晒干水分 2.某省发现部分大米镉超标,镉超标易引起镉中毒。镉元素的核电荷数为48,相对原子质量为112,则镉原子核内中子数是( ) A.48 B.64 C.112 D.160 3.臭氧(O3)、二氧化碳(CO2)、双氧水(H2O2)等都是生产、生活中常用的消毒剂,三种物质中都含有( ) A.氧分子 B.氧离子 C.氧气 D.氧元素 4.以下实验操作正确的是( )
5.下列除去杂质的方法,错误的是( ) A.除去H2中的少最水蒸气:通过浓硫酸 B.除去CO中的少最CO2:通入足量的NaOH溶液,干操 C.除去NaCl溶液中少量的CaCl2:加入适量Na2CO3溶液,过滤 D.除去FeCl3溶液中少量的CuCl2:加入足量的铁屑充分反应后,过滤 6.下图是密闭体系中某反应的微观示意图,“ 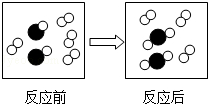 A.参加反应的“ B.反应前后原子种类没有改变 C.反应后该密闭体系中没有单质存在 D.该反应是化合反应 7.科学研究中常用图象来表示两个量(x,y)之间的关系,以使研究的结果变得直观明了。在某温度下,将少量氧化钙加入到一定量的饱和氢氧化钙溶液中。图甲表示整个过程中温度的变化,图乙表示氢氧化钙的溶解度与温度的关系,某同学根据观察和思考,作出了如图丙所示的图象,此图象反映了该过程中( ) 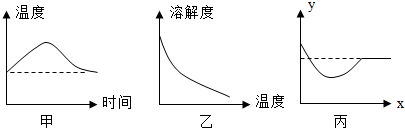 A.溶质的质量与时间的关系 B.溶剂的质量与时间的关系 C.溶质的溶解度与时间的关系 D.溶质的质量分数与时间的关系 8.下列有关说法正确的是( ) A.“春色满园,花香四溢”说明分子在不停地运动 B.空气是由空 C.组成CO、CO2 的元素种类相同,所以它们的化学性质相同 D.气体受热膨胀是因为温度升高气体分子变大 9.下列叙述错误的是( ) A.三大合成材料是指塑料、合成纤维、合成橡胶 B.聚乙烯塑料袋可用加热法封口 C.燃烧法可辨别毛衣的成分是羊毛还是化纤 D.棉花和涤纶都是天然纤维 10.下列有关“化学之最”的叙述中错误的是( ) A.钨是熔点最高的金属 B.最简单的有机物是乙醇 C.金刚石是天然存在最硬的物质 D.空气中含量最多的物质是氮气 11.6月5日是“世界环境日”,以下做法不利于环境保护的是( ) A.工业废水与生活污水处理达标再排放 B.植树造林,禁止乱砍滥伐 C.为了增产,大量施用农药和化肥 D.使用可降解塑料代替传统塑料 卷Ⅱ(非选择题,共76分) 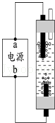 二、填空及简答题(本大题共9个小题;第23小题4分,第24小题3分,其它小题每空1分,共34分) 二、填空及简答题(本大题共9个小题;第23小题4分,第24小题3分,其它小题每空1分,共34分)28.如右图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式为 ,反应前后氯元素化合价的变化是 (填升高或降低);从能量变化角度看,该反应将 能转化为化学能。 29.某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示。
请分析上表,并回答下列问题: (1)该花汁 (填“可以”或“不可以”)作酸碱指示剂。 (2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒。要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的 。 (3)胃酸的主要成分是盐酸,胃舒平[主要成分Al(OH)3]和小苏打常用于治疗胃酸过多症,写出小苏打治疗胃酸过多症时的化学反应方程式 。 (4)石灰水暴露于空气中易 ,溶液表面会形成一层 。 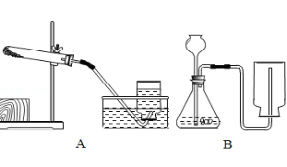 30.根据下列图示回答问题: 30.根据下列图示回答问题: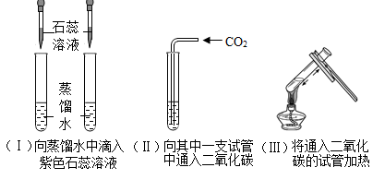 (1)若选用A装置加热高锰酸钾制取氧气,还需补充的一种仪器是 ,反应的化学方程式为 。 (2)实验室若选用装置B制取二氧化碳,则需要改正的一点是 。 (3)用制取的二氧化碳进行试验: ①实验(Ⅱ)中溶液变 色; ②实验(Ⅲ)中加热之后,溶液又变为 色。 31.A、D、F为常见气体,其中F为最轻的气体,B为红棕色固体.它们之间相互反应关系如下图(部分生成物略去),请按要求回答下列问题。 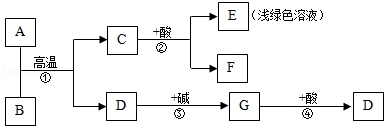 (1)写出E和G的化学式:E 、G 。 (2)反应③的化学方程式: 。 (3)反应②的反应类型是: 。 三、实验探究题(本大题共4个小题;第32小题4分,第33小题6分,第34、35小题各7分,共24分) 35.某同学将光亮的镁条放入滴有酚酞的NaHCO3饱和溶液中,产生大量气泡和白色固体,溶液红色加深。 (一)溶液红色加深,则反应后溶液的碱性 (填“增强”、“不变”或“减弱”)。 (二)为确定气体和固体的成分,该同学进行了如下的探究。 (1) 点燃产生的气体,火焰呈淡蓝色;将燃烧产物通入澄清石灰水中,无现象。则该气体 为 (写化学式)。 (2)对白色固体做出如下猜测并进行实验: 【猜测】 查阅资料1:Mg(HCO3)2能溶于水。 ①白色固体可能是MgCO3; ②白色固体可能是 ; ③白色固体可能是MgCO3和Mg(OH)2。 【实验】 ①取洗净后的白色固体,加入足量的 溶液,观察到 ,则白色固体一定含有MgCO3。 查阅资料2:MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。 ②为进一步确定白色固体的组成,该同学进行了定量实验: 称取干燥的白色固体22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部先通过浓硫酸,浓硫酸增重1.8g,则白色固体中含有 ,再通过碱石灰(氧化钙和氢氧化钠的固体混合物),碱石灰增重8.8g,则固体中各成分的质量比为 。 四、计算应用题(本大题共3个小题;第36小题5分,第37小题6分,第38小题7分,共18分。解答时,要求有必要的文字说明、公式和计算步骤等,只写最后结果不得分) 36.盐水选种是我国古代劳动人民发明的一种巧妙的挑选种子的方法。农业生产上常用质量分数15%﹣﹣20%的氯化钠溶液来选种。为了测定某氯化钠溶液是否符合要求,取该溶液70g,加入一定溶质质量分数的AgNO3溶液100g,恰好完全反应【已知:氯化钠溶液和硝酸银溶液反应生成氯化银(AgCl)沉淀和硝酸钠】。过滤分离出沉淀的质量为28.7g。 (1)反应后所得溶液的质量为 g。 (2)通过计算确定该氯化钠溶液是否符合选种要求?(计算结果精确到0.1% 2018年黔东南中考化学复习题参考答案 一、1.B 2.B 3.D 4.B 5.D 6.C 7.A 8.A 9.D 10.B 11.C 二、28.2NaCl+2H2O 29.(1)可以(2)肥皂水(3)NaHCO3+HCl═NaCl+H2O+CO2↑(4)变质 白膜 30.(1)酒精灯 2KMnO4 (2)将集气瓶正放,用向上排空气法收集(3)①红 ②紫 31.(1)FeSO4(或FeCl2等) CaCO3(或Na2CO3等) (2)CO2+Ca(OH)2=CaCO3↓+H2O (或CO2+2NaOH=Na2CO3+H2O)(3)置换反应 三、35.增强 H2 Mg(OH)2 实验:①稀盐酸 有气泡产生;②Mg(OH)2 ; 84:29或29:84。 四、36 解:(1)141.3(1分) (2)解:设该氯化钠溶液中氯化钠的质量为X。 NaCl+AgNO3=AgCl↓+NaNO3(1分) 58.5 143.5 X 28.7g X=11.7g(1分) 溶液中氯化钠的质量分数= 答:该氯化钠溶液符合选种要求。 5 (责任编辑:admin) |