|
☆☆☆ 点击下载试题 ☆☆☆ 由于格式问题此试题可能会出现乱码的情况 为了方便您阅读请点击右上角的全屏查看 2018枣庄市中考复习化学练习题 第一部分 选择题(共25分) (每小题只有一个选项符合题意。每小题1分) 1.下列变化中,属于化学变化的是 A.矿石粉碎 B.酒精燃烧 C.汽油挥发 D.冰雪融化 2.下列生活用品中,属于纯净物的是 A.牛奶 B.蒸馏水 C.加碘盐 D.山西陈醋 A.木制桌椅 B.塑料杯托 C.金属表链 D.陶瓷碗 4. (枣庄中考化学)下列食物富含糖类的是 A.鸡蛋 B.黄瓜 C.牛肉 D.米饭 5.下列物质在氧气中燃烧,产生大量白烟的是 A.红磷 B.木炭 C.甲烷 D.铁丝 6.“含氟牙膏”“加碘盐”“铁强化酱油”中的“氟”、“碘”、“铁”指的是 A.分子 B.原子 C.离子 D.元素 7.夏天的傍晚,去散步前往身上喷花露水,蚊子 A.分子之间有间隙 B.分子在不断运动 C.分子由原子构成 D.分子的质量较大 8.下列饮品属于溶液的是 A.蔗糖水 B.牛奶 9.(枣庄中考化学)用分子的相关知识解释下列现象,其中正确的是 A.闻到花香——分子不断运动 B.氧气助燃,氢气可燃——分子的质量不同 C.氢气球在高空膨胀——分子体积变大 D.氢气燃烧生成水——分子间有间隔 10.(枣庄中考化学)下列标 A B C D 11.下列符号表示2个氢原子的是 A.H B.2H C.H2 D.H+ 12.下列物质中含有氧分子的是 A.空气 B.二氧化碳 C.过氧化氢 D.水 13.已知 A.2 B.8 C.10  14.(枣庄中考化学)镁有“国防金属”的美誉。在元素周期表中,镁元素的信息如下图所示,对图中信息解释不正确的是 14.(枣庄中考化学)镁有“国防金属”的美誉。在元素周期表中,镁元素的信息如下图所示,对图中信息解释不正确的是A.原子序数为12 B.元素符号为Mg C.属于金属元素 D.相对原子质量为24.31g 15.下列物质的用途中,利用其化学性质的是 A.干冰用于人工降雨 B.石墨作铅笔芯 C.用铜丝作导线 D.用稀盐酸除去铁锈 16.新型锂离子电池的主要成分是LiFePO4,已知锂(Li)的化合价为+1价,Fe的化合价为+2,则LiFePO4中P的化合价是 A.+2 B.+3 C.+5 D.+6 17.(枣庄中考化学)某花圃所种的花卉缺乏氮元素和钾元素,如果只施用一种化肥,则应施用的是 A.K2CO3 B.KNO3 C.CO(NH2)2 D.Ca(H2PO4)2 18.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示。下列说法正确的是  A.t1℃时,甲溶液中溶质的质量分数一定等于乙溶液 A.t1℃时,甲溶液中溶质的质量分数一定等于乙溶液B.降低温度,可使甲的饱和溶液变为不饱和溶液 C.t2℃时,分别在100 g水中加入50 g 甲、乙, 同时降温至t1℃,甲、乙溶液均为饱和溶液 D.将t2℃时甲的饱和溶液降温至t1℃,溶液质量不变 19.(枣庄中考化学)下列有关生活、环境、资源等问题叙述不正确的是 A.pH<5.6的雨水称为酸雨 B.“温室效应”主要是由CO2等气体引起的 C.地球表面约71%被水覆盖,因此淡水资源丰富 D.PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性 20.下列物质的用途中,利用其化学性质的是 A.干冰用于人工降雨 C.氢氧化钠用作干燥剂 D.大理石用作建筑材料 21.从电解水反应的微观示意图中 A.化学反应是分子的重新组合 B.化学反应前后原子的数目增多 C.该反应说明水由氢气和氧气组成 D.该反应的基本反应类型为分解反应 22.(枣庄中考化学)下列物质暴露在空气中,质量增加且变质的是 A.浓硫酸 B.浓盐酸 C.氢氧化钠 D.石灰石 23.下列各组气体中,不能用燃着的木条区分的是 A.氧气和空气 B.二氧化碳和氮气 C.甲烷和空气 D.一氧化碳和二氧化碳 24.下列做法不正确的是 A.电器失火后首先要切断电源 B.进入久未开启的地窖前先做灯火实验 C.厨房煤气泄漏后立即打开抽油烟机 D.燃放烟花爆竹时,远离人群和可燃物 25.某同学对下列四个实验都设计了两种方案,其中方案1不合理、方案2合理的是
〖生活现象解释〗 26.(4分)从①氮气 ②氧气 ③生石灰 ④熟石灰 ⑤碳酸氢钠 ⑥碳酸钙6种物质中选择适当的物质填空。 (1)可用作焊接金属的保护气的是 。 (2)可用作补钙剂,其补钙原理是 (用化学方程式表示)。 (3)可用作食品干燥剂的是 。 (4)制作松软可口的馒头时常加入发酵粉,其主要成分是 。 27.((枣庄中考化学)4分)想要做出绿色的包子。 (1)可将菠菜榨汁,通过 操作将菜渣去除,用菜汁和面。 (2)发面过程中需要加入碳酸氢钠,碳酸氢钠俗称 ,碳酸氢钠还可用于治疗胃酸过 多,其原理是 (用化学方程式表示)。 (3)调馅时使用铁强化酱油,人体“补铁”可以预防_______(填序号)。 A.骨质疏松 B.缺铁性贫血 C.甲状腺肿大 D.营养不良 28.(3分)“绿色出行,低碳生活”是公租自行车倡导的主题。据统计,目前通州区共投入运行营15000辆自行车。 (1)右图自行车所标示的各部件中,属于有机合成材料的是_______(填序号)。 (2)公共自行车的闸线是钢丝,由钢锭制 成钢丝说明金属材料具有_______性。 (3)车架表面喷漆防锈蚀的原理是_______。 29.(枣庄中考化学)(4分)水是我们每天都需要的物质。  (1)右图是实验室电解水实验的装置图,反应的化学方程式为 , (1)右图是实验室电解水实验的装置图,反应的化学方程式为 ,a试管中产生的气体为 。 自然界中的水需净化后饮用,活性炭常用于净化水,其主要 作用是 。 (3)水常用于灭火,其灭火原理是 。 30.(5分)金属和金属材料在生活中有广泛用途。 (1)高铁列车的开通,使人们的出行更加方便、快捷。 ①列车电路中的导线大多是用铜制的,这是利用了铜的延展性和 性。  ②列车车体使用的金属材料是用一氧化碳还原赤铁矿炼制的,其反应的化学方程式为 。 ②列车车体使用的金属材料是用一氧化碳还原赤铁矿炼制的,其反应的化学方程式为 。车体表面喷漆除美观外,主要是为了防止外壳生锈,其防锈原理是 。 ③铝热剂是修建铁路时常用的焊接材料,其反应原理 是在高温下,铝与四氧化三铁反应得到熔融的铁与一种氧 化物,该反应的化学方程式为 。 (2)已知M、N、R三种金属存在如下反应:R+NCl2= N+ RCl2 ,M+ RCl2 = R + MCl2,则M、N 、R三种金属的活动性由强到弱的顺序为 。 31.(枣庄中考化学)(5分)生活中常用的清洗剂。
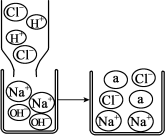 (1)若将洁厕灵与炉具清洁剂混合,可以发生右图所示的化学反应。 (1)若将洁厕灵与炉具清洁剂混合,可以发生右图所示的化学反应。该反应的化学方程式为 , 图中a微粒的微观示意图为 。 (2)高效去污粉中加入足量的洁厕灵,发生反应的化学方程式为 。 (3)消毒液成分中, 中 Cl元素的化合价为+1价。工业上将氯气(Cl2)通入烧碱溶液中可制取消毒液,该反应的化学方程式为 。 〖科普阅读理解〗 32. (枣庄中考化学)(5分)阅读下面科普短文。 锂电池是指电极材料含金属锂或含锂化合物,使用非水溶液做离子导体的电池。银白色的金属锂是所有金属中最轻的一种,它的化学性质活泼,常温下就能和空气中的氧气化合成氧化锂;锂还能和水剧烈反应变成氢氧化锂(LiOH),同时放出一种可燃性气体。 由于锂离子电池中包含的电解液多含有机物,普遍存在易燃问题,在过充、过放、短路及热冲击等滥用的状态下,电池温度迅速升高,常常会导致电池起火,甚至爆炸。因此,目前大多数数码产品都会配备相应的保护元件,当检测到电池到达满电状态,会自动切断充电电路。 依据文章内容, (1)金属锂的物质性质有 (答一条即可)。 (2)锂离子电池由 构成。 (3)锂离子电池负极材料为LiCoO2,其中Li为+1价,则Co的化合价为 。 (4)锂电池使用非水溶液做离子导体的原因是 (用化学方程式表示)。 (5)安全使用锂离子电池的措施有 。 33. (枣庄中考化学)(5分) 根据下图回答问题:  (1)仪器a的名称是__________。 (2)用 A与C连接制取气体的化学方程式为 。 (3)用C装置收集气体的依据是 (4)D装置用来探究燃烧的条件,当观察到 时,说明可燃物燃烧温度需要达到着火点。 (5)E装置中水的作用是 。 34.(枣庄中考化学)(4分)化学小组的同学用干冰做了一组有趣的实验。 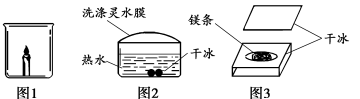 (1)将一小块干冰放入图1所示烧杯中,观察到的现象是 ,产生该现象的原因是 。 (2)将干冰放入盛有少量热水的玻璃碗中,用绳子蘸取洗涤灵水在碗口轻轻刮一层薄膜,一段时间后观察到如图2所示的现象,水膜鼓起的原因是 。 (3)在干冰中间挖一个槽,将镁条点燃放入槽内(如图3所示),在上方盖一块干冰,观察到镁条继续燃烧,有黑白相间的固体生成,该固体的成分可能是 。 〖实验原理分析〗 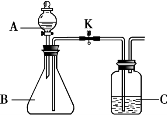 35. (枣庄中考化学)(5分)化学小组同学用下图所示装置(夹持仪器已略去)做兴趣实验。 35. (枣庄中考化学)(5分)化学小组同学用下图所示装置(夹持仪器已略去)做兴趣实验。(1)若A中盛放足量浓氢氧化钠溶液,B中盛放二氧化碳气体,C中盛放稀盐酸。将分液漏斗中的浓氢氧化钠注入B中,此时B中发生反应的化学方程式为 ,一段时间后打开止水夹K,观察到的现象是 。 (2)若A中盛放足量的________,B中盛放蒸馏水,C中盛放某红色溶液。打开止水夹K,将A中物质滴入B中充分接触后,可观察到B中液体进入C中,C中红色溶液变成无色。C中盛放的物质可能是_____________,一段时间后可能观察到的现象是 。 〖科学探究〗  36.(枣庄中考化学)(6分)某同学在做“氢气在空气中燃烧”实验时,对生成物的成分产生了质疑:水和过氧化氢具有相同的组成元素,那么氢气在空气中燃烧除生成水外,是否还有过氧化氢生成呢?带着疑问,该同学利用如图所示实验装置进行了以下探究。 36.(枣庄中考化学)(6分)某同学在做“氢气在空气中燃烧”实验时,对生成物的成分产生了质疑:水和过氧化氢具有相同的组成元素,那么氢气在空气中燃烧除生成水外,是否还有过氧化氢生成呢?带着疑问,该同学利用如图所示实验装置进行了以下探究。【提出猜想】氢气在空气中燃烧除生成水,还有过氧化氢生成。 【查阅资料】 ①在一 ②过氧化氢溶液能使无色的淀粉碘化钾溶液变蓝色。 【实验探究】
【反思评价】实验中将氢气燃烧的火焰对着冰,冰的作用是 。 A.有利于防止生成的过氧化氢分解 B.使生成的过氧化氢溶入冰融化成的水中,便于收集 C.创设低温环境,使部分氢气燃烧产生一定量的过氧化氢 【拓展分析】(枣庄中考化学)除氢气和氧气反应会生 〖实际应用定量分析〗 37.(枣庄中考化学)(7分)柠檬酸(C6H8O7)是一种常见的有机酸,用棉花蘸取柠檬酸溶液,擦洗杯子内的茶渍。  (1)柠檬酸中碳、氢元素的质量比为 ,氧元素质量分数的计算式为 。 (1)柠檬酸中碳、氢元素的质量比为 ,氧元素质量分数的计算式为 。(2)现配制200 g质量分数为40%的柠檬酸溶液,实验操作如下: ①称量 g柠檬酸固体;②用量筒量取 mL水(ρ水≈1 g/cm3);③溶解;④装瓶、贴标签:在右图的标签中填上相应的内容。 整个实验过程中用到的玻璃仪器有 。 (3)若将50g质量分数为40%的柠檬酸溶液,稀释成10%的柠檬酸溶液,需加水 g。 38.(3分)在质量为150 g的烧杯中加入100 g过氧化氢溶液,再向其中加入2 g二氧化锰。充分反应后,称得烧杯和剩余物质总质量 (责任编辑:admin) |


