|
☆☆☆ 点击下载试题 ☆☆☆ 由于格式问题,部分试题会存在乱码的现象,请考生点击全屏查看! 可能用到的相对原子质量: H—1 C—12 N—14 O—16 Ca—40 Cl—35.5 Zn—65 Fe—56 Ag—108 第Ⅰ卷(选择题 16分) 一、选择题(下列各题中只有一个正确选项。其中,1~4小题各1分,5~10小题各2分,共16分。请将答案填写在第Ⅱ卷的答题栏里。) 1. 下列图中所示过程发生化学变化的是( ) 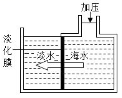 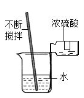 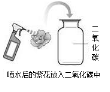 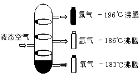 A. B. C. D. ①3Ag ②Fe3+ ③SO3 ④NaNO2 ⑤3O2﹣ ⑥3P2O5 A. 表示离子所带电荷数的是②⑤ B. 表示分子个数的是① C. 表示一个分子中原子个数的③⑥ D. 表示化合价数值的是④ 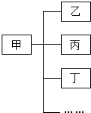 3. 分类是化学学习和研究的一种常用科学方法,小红用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁……下列关系中,有错误的一组是( ) 3. 分类是化学学习和研究的一种常用科学方法,小红用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁……下列关系中,有错误的一组是( )A. 盐 食盐、纯碱、高锰酸钾 B. 合金 不锈钢、焊锡、生铁 C. 溶液 碘酒、糖水、生理盐水 D. 干燥剂 石灰石、浓硫酸、生石灰 4. 从分子的角度分析并解释下列事实,说法不正确的是( ) A. 冰不容易分割,水易分割 冰中水分子间作用力大 B. 糖水是混合物 由不同的分子构成 C. 可燃冰变为天然气 状态变化,分子大小随之变化 D. 水通电分解 分子在化学变化中可分 A. 铁丝在氧气中燃烧 4Fe+3O2 2Fe2O3 6. a、b、c 三种物质的溶解度曲线如下图所示。取等质量t2℃的 a、b、c 三种物质的饱和溶液,分别蒸发等量水后恢复至t2 ℃。下列说法不正确的是( ) A. 原饱和溶液中,溶质的质量分数 a>b=c B. 恢复至 t2℃时,析出溶质的质量 a>b=c C. 恢复至t2℃时,三种溶液一定都是饱和溶液 D. 若继续降温至 t1℃,三种溶液一定都是饱和溶液 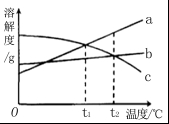 7. 把二氧化碳、一氧化碳、氢气和氮气混合气体通过石灰水,灼热的氧化铜(假设每个过程中发生的化学反应充分),冷却后留下的气体是( ) 二氧化碳和氮气 B. 氮气和水蒸汽 C. 一氧化碳和二氧化碳 D. 氮气和氢气 8. 将一定质量的Zn粉加入一定质量的AgNO3和Fe (NO3)2的混合溶液,得到的固体质量随时间的变化关系如图所示.下列说法不正确的是( ) A. 当反应进行到t时,所得金属固体中的物质至少有两种 B. 当反应进行到t时,取反应后的滤液滴加稀盐酸,有白色沉淀产生 C. 当反应进行到t时,此时取滤渣滴加稀盐酸,一定有气泡产生 D. 当反应进行到t时,取反应后的滤液观察,滤液呈浅绿色 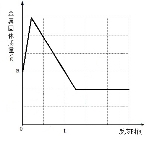 9. 下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是( )
10. 某化学课外活动小组在准备实验时配制了Na2SO4、Na2CO3、BaCl2、HCl种溶液,因没及时贴标签,将其混淆。为将它们区别开来,把四种溶液编号为①②③④,并进行了下面的实验:
按①②③④的顺序,由以上实验现象可以确定它们依次是 ( ) A. BaCl2、Na2CO3、Na2SO4、HCl B. HCl、Na2SO4、Na2CO3、BaCl2 C. Na2SO4、BaCl2、Na2CO3、HCl D. Na2CO3、BaCl2、HCl、Na2SO4 选择题答题卡:(请把正确选项填入下表内)
第Ⅱ卷(非选择题 34分) 二、填空与简答(共16分) 11.(4分)化学用语是学习化学的重要工具,是国际通用的化学语言。请用化学用语回答下列问题: (1)铝在空气中生锈的产物的化学式 。 (2)草木灰和纯碱溶液中都存在的离子 。 (3)硝酸铵中氮元素的化合价 。 (4)通过化合反应生成水的化学方程式 。 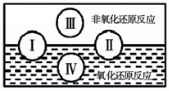 13. (3分) 如图A~D是四种粒子的结构示意图,E是铈元素在元素周期表中的信息:(多个答案的必须选全) 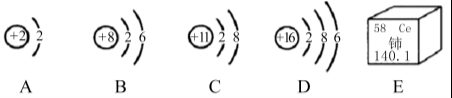 (1)在A~D中,位于同一周期的元素是 (填字母); (2)在A~D中,具有相对稳定结构的粒子是 (填化学符号); (3)铈的相对原子质量为 。 14.(4分)一包白色粉末,由NaOH、Na2SO4、CaCO3、CuCl2、BaCl2、NaCl中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验: (1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到沉淀和无色滤液。 (2)取实验(1)滤出的沉淀,向其中加入足量的盐酸,沉淀全部溶解,产生无色气体,同时溶液变成蓝色。则原白色粉末中一定含有 。 根据上述实验可推断:原白色粉末的组成有 种可能。 为进一步探究原白色粉末的组成,取实验(1)得到的滤液,向其中通入二氧化碳,产生白色沉淀,则可推断原白色粉末的组成为 或 。 15. (1分)“科学认识”确保健康,生活中的下列做法,你认为合理的是 。 A.家居装饰好后可使用活性炭吸附一些有异味的物质 B.发霉的大米蒸熟后可放心食用 C.为防止骨质疏松,可以多吃奶类、豆制品、虾皮等食物 D.合格的火腿肠中含有防腐剂亚硝酸钠,因此也不能食用 E. 市售香烟通常装有过滤嘴,所以吸烟对人体无害 三、实验与探究(共12分) 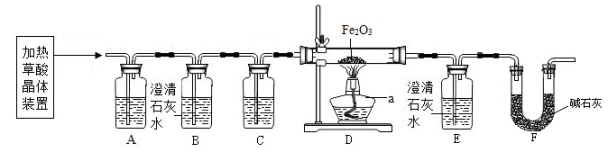 16.(7分)某实验小组同学用加热草酸晶体制得CO,并利用CO来完成炼铁实验,请你参与过程分析。 16.(7分)某实验小组同学用加热草酸晶体制得CO,并利用CO来完成炼铁实验,请你参与过程分析。【查阅资料】 (1)实验室常用氢氧化钠溶液除去二氧化碳,用澄清石灰水检验二氧化碳。 (2)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,化学方程式为: 【问题讨论】 实验室提供下列仪器供选择使用:①试管 ②烧杯 ③集气瓶 ④蒸发皿 ⑤酒精灯⑥带导管的橡皮塞 ⑦铁架台(含铁夹) ,其中你认为在加热分解草酸晶体的装置中,需要用到的仪器有 (填序号)。 进入D装置的气体是纯净、干燥的CO,则A,C装置中的试剂依次是 、 (填名称); (3)写出A装置中发生反应的化学方程式 ; (4)B装置的作用是 ; (5)证明草酸晶体分解产物中存在CO的现象是 ; 【实验评价】 反思:请指出上述实验装置的一个明显缺陷 。 17.(5分)已知在某化肥K2SO4样品中可能混入了NH4Cl、NH4NO3、K2CO3三种物质中的一种或多种,为推测混入的物质种类,现按图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全进行)。 试根据实验过程和发生的现象填写以下空白: 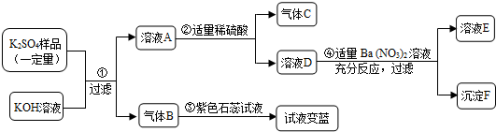 (1)常温下,气体B水溶液的pH 7(填“大于”“小于”“等于”之一)。 (2)实验步骤②的现象证明可能混入的三物质中,一定存在的物质是 。 (3)根据上述实验,已经证明了溶液E中存在的溶质有(写化学式) 。 (4)仅根据上述实验现象, NH4Cl、NH4NO3、K2CO3三种物质中,还不能确定是否混入化肥K2SO4样品中 (5)要进一步推理化肥样品中的物质,可用溶液E再实验,请简要说明实验操作步骤、发生的现象及结论 四、计算与应用(共6分) 18. (2分)荷叶茶具有清凉败火,消脂润肠等功效,因减肥效果明显,所以深受人们喜爱。荷叶碱(化学式为C19H21NO2)是荷叶中的一种生物碱,为荷叶中的主要降脂活性成分;请你计算: (1)荷叶茶中氢元素与氧元素的质量之比是 ; (2)荷叶茶中碳元素的质量分数是 (精确到0.1%)。  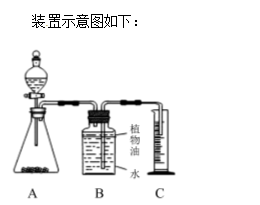 19. (4分)某化学小组为测定一瓶失去标签的盐酸的溶质质量分数,分成甲、乙两组,分别用不同的方法进行测定。实验设计: 甲组:取纯净碳酸钙粉末5g于烧杯中,加入20g该盐酸溶液,充分反应后,过滤、洗涤、干燥,称量得剩余固体3g。 乙组:取纯 【数据处理】: (1)你认为哪一种实验方法不准确,请说明原因 。 (2)请利用你认为实验合理的一组数据计算该盐酸的溶质质量分数。(写出计算过程) 一、选择题(下列各题只有一个正确选项。其中,1-4小题各1分,5-10题各2分,本大题共16分。)
11.(1) Al2O3 (2) CO32- (3)NH4NO3 (4) 2H2+O2 2H2O 12. 分解反应;NaOH + HCl = H2O + NaCl(其它答案合理即可); Ⅳ; 氧化。 13. (1) CD (2) He、Na+ (3) 140.1 14. NaOH、CaCO3、CuCl2; 6 ; NaOH、CaCO3、CuCl2、BaCl2; NaOH、CaCO3、CuCl2、BaCl2、NaCl 15. AC 三、实验与探究(共12分) 16. (1) ①⑤⑥⑦ (2) 氢氧化钠 浓硫酸 (3) 2NaOH+CO2=Na2CO3 +H2O (4)检验一氧化碳中是否含有二氧化碳 (5)D装置中的红色粉末慢慢变成黑色 【实验评价】没有尾气处理装置 17. (1)大于 (2)K2CO3 (3)KNO3 (4)NH4Cl、NH4NO3 (5)向溶液E中加入硝酸银,如果有白色沉淀生成,说明样品中含有NH4Cl,可能含有NH4NO3;如果没有白色沉淀,则样品中含有NH4NO3,不含有NH4Cl。 四、计算与应用(共6分) 17. (1)21:32 (1分) (2)77.3% (1分) 18.(1)乙组数据不准确,原因:测量的水的体积小于生成气体的体积; B、C之间的导管内实验前无水,实验后有水;内外气压相同时,二氧化碳无法将相应体积的水压入量筒;二氧化碳可能溶解在A中反应后的溶液中。(1分,合理答案均可给分) (2)根据甲组数据计算 解:设参加反应的HCl质量为x ,消耗碳酸钙质量为5g-3g=2g 2HCl+CaCO3=CaCl2+H2O 73 100 x 2g 73/x=100/2g x =1.46g (1分) 盐酸的溶质质量分数为:1.46g/20g×100%=7.3% (1分) 答:盐酸的溶质质量分数为7.3%。 (责任编辑:admin) |
