|
物质的制备、性质和检验 练习题
1.实验室中准备有下面主要仪器:大试管、带导管的单孔塞、药匙、镊子、水槽、集气瓶、玻璃片、酒精灯、铁架台九种,如果药品选用合理,仪器可以选其中的几种,能制取的气体有 ( )
A.只有氧气 B.只有二氧化碳
C.氢气和二氧化碳 D.氧气、氢气和二氧化碳
2.含有少量水蒸气的下列气体,既可以用固体氢氧化钠干燥,又可用浓硫酸干燥的是 ( )
A.一氧化碳 B.二氧化碳 C.二氧化硫 D.氯化氢
3.只用下列试剂中的一种,就能鉴别氢氧化钠,氢氧化钙和稀盐酸三种无色溶液,它是( )
A.酚酞试剂 B.氯化钡溶液
C.石蕊试剂 D.碳酸钠溶液
4.检验氢气的纯度时,用右手拿充满气体的试管底部,用拇指堵住管口,移近火焰时应( )
A.管口向下
B.管口向上
C.试管保持水平,管口向前
D.试管保持水平,管口向后
5.要证明氧化钙能跟水发生反应,只需选用下列试剂中的 ( )
A.稀硫酸 B.氢氧化钾
C.氯化钡 D.酚酞试剂
6.实验室用锌和盐酸反应制取氢气。在制得的氢气中常含有少量的水蒸气和氯化氢气体。为了得到纯净的氢气,应选用的洗气装置(左边试管中装有NaOH溶液,右边试管中装有浓H2SO4)是( )
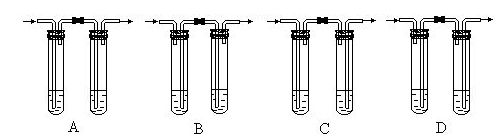
7.证明一白色粉末是硫酸铜,在以下四种方法①取少量溶于水,加NaOH溶液,有蓝色沉淀生成②取少量溶于水,加稀H2SO4不反应③取少量溶于水,加Ba(NO3)2溶液和稀HNO3,有白色沉淀生成。可以选用的是 ( )
A.①② B.②③ C.③ D.①③
8.除去氧化铜中少量杂质铜的最好方法是 ( )
A.通入氢气,加热
B.在空气中加热
C.通入CO,加热
D.加入少量稀盐酸后加热
9.实验室常用于检验碳酸盐的方法是 ( )
A.加入氯化钡溶液,产生白色沉淀
B.加入石灰水,产生白色沉淀
C.加入稀盐酸,产生使石灰水变浑浊的气体
D.放入水中,不溶解的是碳酸盐
10.托盘天平两端各放一小烧杯,其中加入相同浓度,相同质量的盐酸(足量),使左、右两盘平衡,在左盘加入5.6g氧化钙完全反应,若使天平继续保持平衡,应向右盘加碳酸钙的质量是( )
A.5.6g B.4.4g C.10g D.14.4g
11.某溶液pH=9,为使其pH降到6以下,应滴加 ( )
A.盐酸 B.氢氧化钠溶液
C.水 D.食盐水
12.要除去铜粉里混有的少量锌粉,可加 ( )
A.硫酸镁溶液 B.稀硫酸
C.水 D.碳酸铜
13.用实验证明铜、银两种金属的化学活动性顺序,应选用的试剂是 ( )
A.硫酸钠溶液 B.硝酸银溶液
C.硫酸锌溶液 D.稀硫酸
14.现有NaCl、Na2CO3、Na2SO4三种无色溶液,为鉴别它们最好选用 ( )
A.AgNO3溶液 B.石蕊溶液
C.AgNO3溶液和盐酸 D.BaCl2溶液和稀HNO3
15.若鉴定某无色溶液是盐酸应选用的试剂有 ( )
A.紫色石蕊试液
B.硝酸银溶液和稀硝酸
C.无色酚酞试液和硝酸银溶液
D.紫色石蕊试液,硝酸银溶液和稀硝酸
16.只用一种试剂区别Ba(NO3)2、NaCl、KOH三种无色溶液时,可选用的试剂是 ( )
A.碳酸钠溶液 B.盐酸
C.硫酸 D.硫酸铜溶液
17.在盛有下列固体的烧杯内,加入足量稀盐酸,得到无色溶液的是 ( )
A.CuO B.Fe(OH)3
C.Na2CO3 D.Cu(OH)2
18.下列各组物质中,经混合后,溶液质量不发生改变的是 ( )
A.氯化钠溶液和硝酸银溶液
B.碳酸钠溶液和盐酸
C.硝酸钡溶液和硫酸锌溶液
D.氢氧化钠溶液和硝酸
19.鉴别硫酸和盐酸最好选用 ( )
A.氯化钡溶液 B.硝酸银溶液
C.碳酸钠溶液 D.石蕊试液
20.使酚酞试液变红的溶液使石蕊试液呈 ( )
A.红色 B.无色 C.蓝色 D.紫色
21.鉴别石灰水和氢氧化钠溶液最好选用 ( )
A.石蕊试剂 B.酚酞试剂
C.碳酸钾 D.氯化钡溶液
22.现有四组气体(1)N2和CO2 (2)O2和CO2 (3)CO和CO2 (4)CO2和CH4能把上述四组气体用一种试剂或方法就能区别开的是 ( )
A.用燃着的木条 B.用带火星的木条
C.用澄清的石灰水 D.用酚酞试剂
23.在相同条件下,某气体密度比空气小,在水中易溶解,收集该气体应采用 ( )
A.排水集气法
B.向下排空气集气法
C.向上排空气集气法
D.既可用排水集气法,又可用排气集气法
24.盛放下列物质的容器不需密封的是 ( )
A.石灰水 B.石灰石
C.固体氢氧化钠 D.氨水
25.将符合下图装置设计意图的序号填入括号中。
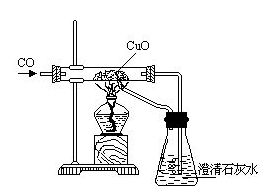
设计意图:①说明CO具有还原性②既说明CO具有可燃性,又充分地利用了能源③说明CO氧化后的产物是CO2④有效地防止了有剧毒的CO对空气的污染。其中符合的是 ( )
A.只有① B.①②③ C.③和④ D.以上都符合
26.能区别稀硫酸、水和烧碱三种液体的试剂是 ( )
A.锌粒 B.无色酚酞试液
C.氯化钡溶液 D.紫色石蕊试液
27.在下列图示实验中,漏斗或导管口位置正确的是 ( )
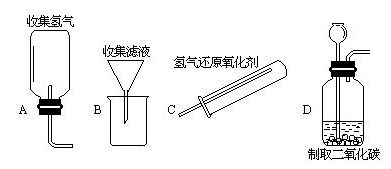
28.要检验某氢氧化钠溶液吸收了空气中的二氧化碳,可以向少量该溶液中加入 ( )
A.过量盐酸 B.过量食盐水
C.几滴石灰水 D.几滴石蕊试液
29.今有A、B、C、D、E五种装置(胶塞、导管可自由选用),请按下列要求回答:
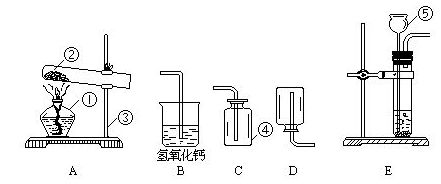
(1)写出①—⑤的名称:①______②______③______④______⑤______
(2)实验室制取并收集氧气时应选择______和______相连接;制取并收集氢气时应选择______和______相连接;制取二氧化碳时应选择______和______相连接。
(3)做木炭还原氧化铜并检验生成的气体实验,应选用______和______装置,实验完成时的现象是______。 ( )
30.水煤气的主要成分是:H2、CO、N2、CO2和水蒸气,把该混合气体依次通入烧碱溶液、灼热的氧化铜、澄清的石灰水和浓硫酸,最后剩余的气体是______。
31.某厂实验室有甲、乙两个药品橱,某中甲橱中已存入有铜、锌,乙橱是空的,现有碳酸钙、浓硫酸、烧碱、浓盐酸、氧化铜,应该分别把它们放入哪个橱中?其中试剂瓶口一定要密封的是哪些化学药品?
甲橱:锌、铜______________________________。
乙橱:______________________________。
需要密封保存的是______________________________。
32.将A、B、C三种钠的正盐溶液,各取少许放在三支试管中,分别滴BaCl2溶液,C无现象,A、B都有白色沉淀生成。在生成的白色沉淀中加入稀硝酸,B无变化,A沉淀消失,并生成无色气体。将无色气体通入澄清石灰水,石灰水变浑浊;另取C溶液少许,加入硝酸银溶液,立即生成白色沉淀。根据上述现象,推断A是______B是______C是______
(均写化学式)
33.有一包固体粉末,可能含有NaCl、Ba(NO3)2、Na2SO4、Na2CO3中的几种,为确定它们做如下实验:
(1)将该固体粉末溶于水,搅拌后有白色沉淀生成;(2)在上述含白色沉淀的溶液中加入稀HNO3,则沉淀全部消失。由此推断固体粉末中肯定有____________,肯定没有____________,可能有____________。
34.有一种无色溶液A,加入硫酸钠溶液充分搅拌过滤,得到白色不溶于硝酸的沉淀B和无色滤液C,如果向C液中加入硝酸银溶液不断搅拌后过滤,又得到不溶于稀硝酸的白色沉淀D和无色溶液E。确定A→E各物质的名称。
A______B______C______D______E______
并写出有关化学方程式________________________
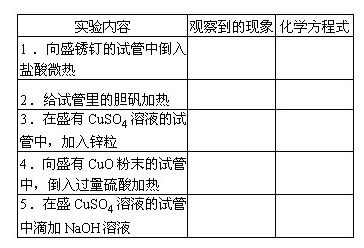
35.填写实验报告
36.在实验室用下图所示装置进行CO和CO2的分离和干燥。现只有稀盐酸、浓硫酸、石灰水,按要求填写下列空白
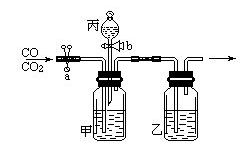
(1)甲中应盛______,乙中应盛______,丙中应盛______。
(2)若关闭活塞b,打开铁夹a,可分离出______,反应的化学方程式为______。
(3)若关闭铁夹a,打开活塞b,又可分离出______,反应的化学方程式为______。
37.水蒸气通过灼热的煤所产生的混合气其主要成分是CO、H2,此外还含有水蒸气和CO2。请用下列装置图设计一个实验,以确认上述混合气中含有CO和H2。
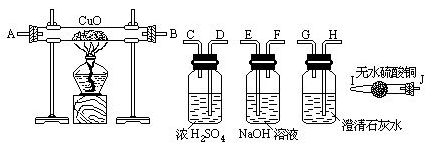
(1)连接上述装置的正确顺序是(填写各接口的字母)
混合气→____________接____________接____________接____________接____________
(2)确认混合气中含有H2的实验现象是__________________
38.只有氯化钡溶液和简单的仪器装置,鉴别稀硫酸和碳酸钠溶液(任意编号为甲、乙溶液)。操作如下:
(1)分别取少量甲、乙溶液于两支试管中,各滴加氯化钡溶液,两支试管中都产生白色沉淀。
下面还要进行怎样的操作,才能把它们鉴别出来。请将鉴别的步骤、现象及最终结论,填写在相应的横线上。
(2)__________________
(3)__________________
39.100g20%的硫酸铜溶液,跟30%的一定量的氢氧化钠溶液恰好完全反应,求反应后溶液里溶质的质量分数。(H=1,O=16,S=32,Na=23,Cu=64)
(责任编辑:admin)
|