|
2012年4月安徽巢湖黄麓中心学校中考化学模拟试题 安徽省巢湖市 谢玉荣 本卷共三大题16小题,满分60分,化学与物理的考试时间共120分钟。 可能用到的相对原子质量: H-1 ,Li-7 ,C-12 , O-16 ,Fe-56 。 一、本大题包括10小题,每小题2分,共20分。每小题的4个备选答案中只有一个符合题意,请将你选出的答案序号填在题后括号内。 1.某科学家在一次化学论坛会上提出 “化学不是问题,化学解决问题”的观点,则下列叙述不合理的是【 】 A.利用化学合成药物,保障了人体健康 B.利用化学开发新材料,改善人类生存条件 C.利用化学保护环境,使人类生活得更美好 D.化学是万能的,能解决世界上所有的问题 2.合理搭配饮食,是我们的健康理念。这是一份早餐搭配:牛奶、面包、黄油。这份早餐搭配中缺失的营养素是【 】 A.油脂 B.维生素 C.糖类 D.蛋白质 3.钒[V]被誉为金属中的“维生素”,其氧化物V2O5中钒元素的化合价是 【 】 A.+1 B.+3 C.+5 D.+7 4. 化学使人类生活更加丰富多彩,如打火机就给人们生活带来了方便,下列有关打火机的主要燃料丁烷[C4H10]的说法不正确的是【 】 A.从性质上看:丁烷具有可燃性 B.从变化上看:丁烷完全燃烧只生成水 C.从组成上看:丁烷由碳、氢两种元素组成 D.从结构上看:一个丁烷分子由4个碳原子、10个氢原子构成 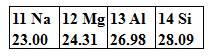 5.右图为元素周期表第三周期的局部。据此判断下列说法中正确的是【 】 5.右图为元素周期表第三周期的局部。据此判断下列说法中正确的是【 】A.硅元素的原子序数为l4 B.镁元素的相对原子质量为l2 C.1个铝原子的质量是26.98g D.它们都属于金属元素 6.下列实验基本操作中正确的是【 】  A.闻气味 B.熄灭酒精灯 C.滴加液体 D.倾倒液体 7.在飞船的火箭推进器中常装有液态肼[N2H4]和过氧化氢[H2O2],它们混合时的反应方程式为:2H2O2 + N2H4=== N2 + nH2O,则下列说法正确的是【 】 A.该反应为置换反应 B.反应前后原子总数发生变化 C.该化学方程式中n=4 D.氮是地壳中含量最高的元素 8.科学家已研制出新型的氧分子O4,对其说法正确的是【 】 A.O4和O2都是由氧元素组成的单质 B.O4是一种新型的化合物 C.1个O4分子中含有2个O2分子 D.O2与O4的性质一定相同 9.图表资料可以为我们提供很多信息,下列关于图表提供的信息或应用的说法中,不正确的是【 】 A.根据相对原子质量表,可查找元素的相对原子质量 B.根据溶解度曲线图,可选择从溶液中获得晶体的方法 C.根据空气质量周报,可知道空气质量级别和首要污染物 D.根据酸、碱、盐的溶解性表,可判断各种酸、碱、盐的溶解度大小 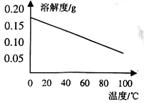 10.右图是熟石灰的溶解度曲线,下列说法正确的是 【 】 10.右图是熟石灰的溶解度曲线,下列说法正确的是 【 】A.熟石灰属于易溶物 B.任何固体的溶解度都是随温度的升高而变大 C.石灰水中溶质的质量分数随温度的升高而变大 D.把20℃时澄清的饱和石灰水升温到100℃溶液变浑浊 二、本大题包括5小题,共34分。 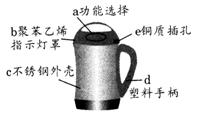 11.(6分)右图是家用豆浆机,请根据图回答下列问题: 11.(6分)右图是家用豆浆机,请根据图回答下列问题: (1)制作材料中属于金属材料的是 ,(填一种) (2)属于合成材料的是 (选填一种物质编号), (3)传统的生豆浆是用石磨来打磨的,打磨的过程是 变化, (4)用操作将黄豆渣分离的方法类似于我们实验中的 操作, (5)该豆浆机不能接触酸性物质,请用化学方程式解释 12.(4分)为测定氯化钠和碳酸钠固体混合物中氯化钠的质量分数,有以下两个实验方案: (1)方案1: 请问:①操作的名称是 。要计算样品中氯化钠的质量分数,实验中必须测量的数据是:碳酸钡的质量和 ; ②若过滤所得固体未经洗涤即烘干称量,测得样品中氯化钠的质量分数将 。(填“偏大”、“偏低”或“不变”) (2)方案2:通过测定样品和足量硫酸溶液反应产生气体的质量来计算样品中氯化钠的质量分数。若测得各物质的质量(g):样品质量为a,所用硫酸溶液质量为b,完全反应后混合溶液质量为c,则生成气体的质量为 g。(用a、b、c表示) 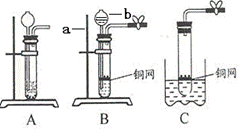 13.(9分)右图是某研究性学习小组设计的几种装置,请你分析并回答下列问题: 13.(9分)右图是某研究性学习小组设计的几种装置,请你分析并回答下列问题: (1)图中标号仪器为:a ,b (2)装置A可用作实验室制取O2或CO2的发生装置,用此装置制取O2的化学方程式是 。 (3)某同学从装置A得到启发,在装置A的基础上增加了隔离铜网改成装置B来制取氢气,又用一支底部有一个小洞的试管和矿泉水瓶组合成装置C(夹持仪器都略去)。则B与A相比优点是 ,C与B相比不同之处是 ;而装置B显示的化学反应状态为 (填“进行中”或“已停止”)。 (4)用装置C制取CO2时若将铜网改用铁丝网做成,则产生的后果是 ,说明金属活动性Fe Cu(填“=”或“>”或“<”) 14.(8分)化学课后,某班同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究: 【提出问题1】 该氢氧化钠溶液是否变质了呢? 【实验探究1】
【提出问题2】 该氢氧化钠溶液是全部变质还是部分变质呢? 【猜想与假设】 猜想1:氢氧化钠溶液部分变质。 猜想2:氢氧化钠溶液全部变质。 【查阅资料】(1)氯化钙溶液呈中性。 (2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl 【实验探究2】
【实验结论】 该氢氧化钠溶液 (填“部分”或“全部”)变质。 【反思与评价】(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式: 。 (2)上述【实验探究2】中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案 (填“可行”或“不可行”)。 【理解与应用】 氢氧化钠溶液容易变质,必须密封保存。实验室必须密封保存的药品还有很多,试另举一例: 。 15.(7分)某化学小组对一包干燥的红色粉末组成进行探究。请你参与并回答有关问题。 【教师提醒】它由Cu 、Fe2O3二种固体中的一种或两种组成。 【提出猜想】红色粉末可能的组成有:①只有Cu;②只有 ;③是 。 【资料获悉】Cu在FeCl3溶液中发生反应:2FeCl3+Cu = 2FeCl2+CuCl2 【实验探究】(1)甲同学取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解。甲同学认为可以排除猜想中的①和③,而乙同学认为只能排除猜想①,你认为 的观点正确(填“甲”或“乙”)。 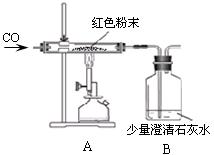 (2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表: (2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按右图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
【交流讨论】 (1)在装置A中先通CO气体的作用是 。 (2)写出A装置中发生反应的化学方程式 ;实验中观察到A装置中的现象为 。 (3)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处? 不需要,理由是因为一直通入CO气体,B中溶液不会倒吸到A装置中。(答对下面(4)与【反思评价】两小题将奖励4分,但全卷总分不超过60分) (4)选择I组的实验数据计算来确定红色粉末的组成。最终计算结果表明:该红色粉末的组成是猜想中的第 组(填序号)。(2分) 【反思评价】丁同学指出:从环保角度,上图装置有严重不足之处。你认为应该如何改进? 。(2分) 三、本大题共6分 16.(6分)氢化锂(LiH)为玻璃状无色透明固体,军事上用作氢气发生来源,反应的化学方程式为:LiH+H2O=LiOH+H2↑。计算80g氢化锂与足量的水反应生成氢气的质量。 2012年安徽巢湖黄麓中心学校中考模拟二化学试题参考答案 一.本大题包括10小题,每小题2分,共20分。
二.本大题包括5小题,共34分 11.(6分)(1)铜或不锈钢(1分)(2)b或d(1分)(3)物理(1分)(4)过滤(1分) (5)Fe+2HCl=FeCl2+H2↑或Fe+H2SO4=FeSO4+H2↑(2分)(答案合理就可) 12.(4分)(1)① 溶解(1分)样品质量(1分)② 偏低(1分)(2)a+b-c(1分) 13.(9分)(1)a铁架台(1分),b长颈漏斗(1分) (2)2H2O2 没有长颈漏斗(利用废旧仪器)(1分);已停止。(1分) (4)所得气体不纯净(或CO2中混有H2)(1分); >(1分) 14.(8分)【实验探究1】有气泡冒出。 (1分) 【实验探究2】(白色)沉淀(1分) 氢氧化钠(或NaOH)(1分) 【实验结论】 部分(1分) 【反思与评价】 CO2+2NaOH=Na2CO3+H2O( 【理解与应用】 浓盐酸(或浓硫酸、或澄清石灰水其他合理答案均可)(1分) 15.( 7分+4分) 【提出猜想】② Fe2O3 (1分) ③ Cu 、Fe2O3的混合物(1分) 【实验探究】(1)乙 (1分) 【交流讨论】 (1)排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸)(1分) (2) 3CO + Fe2O3 (4) ③(2分) 【反思评价】在B装置后放一燃着的酒精灯将剩余气体烧掉(或用塑料袋收集等)。(2分) 16.【解】设:生成氢气的质量为X。 1分 LiH + H2O = LiOH + H2↑ 8 2 1分 80g x 1分 X = 20g 1分 答:生成氢气的质量为20g。 1分 (责任编辑:admin) |
