|
☆☆☆ 点击下载试题 ☆☆☆ 请点击全屏查看 湖北省荆门市2017年中考化学试卷 一、选择题. 1.下列变化,一定发生了化学变化的是( ) A.冰雪融化 B.用活性炭除去水中的色素和异味 C.矿石粉碎 D.燃放烟花 【答案】D 2.(2017荆门化学)下列事实的结论或解释中,不正确的是( ) A.水受热变成水蒸气后体积变大﹣﹣受热后水分子的体积变大 B.二氧化碳和一氧化碳的化学性质不同﹣﹣它们的分子结构不同 C.钠原子和钠离子属于同种元素﹣﹣它们的质子数相等 D.原子是化学变化中的最小粒子﹣﹣在化学变化中原子不能再分 【答案】A 3.下列实验操作正确的是( ) A.用胶头滴管向试管中滴加液体时,为防止液体洒出,可将胶头滴管伸到试管口内 B.稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌 C.为避免药品浪费,做完实验后剩余的药品应放回原试剂瓶中 D.实验室用高锰酸钾制氧气并用排水法收集,实验结束时,先撤酒精灯,后把导管移出水面 【答案】B 4.化石燃料燃烧会排放大量的二氧化碳,引起温室效应,一种新的处理方法是将二氧化碳气体通入含有长石(主要成分KAlSi3O8)的水溶液里,其中一种反应的化学方程式是:KAlSi3O8+CO2+2H2O═KHCO3+X+3SiO2↓,下列说法不正确的是( ) A.X是Al(OH)3 B.反应前后各物质中元素的化合价均未发生变化 C.生成物中有一种氧化物 D.该反应中涉及到的元素种类有5种 【答案】D 5.(2017荆门化学)向AgNO3溶液中加入一定量的Mg粉和Cu粉,充分反应后过滤,得到滤渣和蓝色的滤液.关于该滤渣和滤液有下列四种说法:①向滤渣中加入稀盐酸,可能有气泡产生;②向滤液中加入稀盐酸一定有沉淀产生;③滤渣中一定有Ag;④滤液中一定有Cu(NO3)2、一定不含AgNO3、可能有Mg(NO3)2,以上说法中正确的个数为( ) A.1个 B.2个 C.3个 D.4个 【答案】A 6.除去下列物质中少量的杂质,所选用的试剂及操作正确的是( )
【答案】C 7.下列物质的转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反应,不可能全部实现的是( ) A.H2O2→O2→CO2→H2CO3 B.NaOH→NaNO3→Na2CO3→NaCl C.CaCO3→CaO→Ca(OH)2→KOH D.Mg→H2→HCl→AlCl3 【答案】B 二、非选择题. 8.(2017荆门化学)从C、H、O、N、S、Fe六种元素中,选择适当元素组成化学用语,按要求填空. (1)用适当的化学符号和数字填空: ①4个铵根离子 ;②3个三氧化硫分子 . (2)写出符合下列要求的物质的化学式: ①相对分子质量最小的氧化物 ;②菱铁矿石的主要成分 . 【答案】(1)①4NH4+ ②3SO3 (2)①H2O ②FeCO3 9.碳元素是组成许多物质的基本元素,回答下列含碳元素物质的有关问题. (1)倡导“低碳”生活,主要是为了减少 的排放量. (2)检验CO2常用澄清石灰水,写出该反应的化学方程式 . (3)天然气(主要成分是CH4)作燃料 (用化学方程式表示). (4)为减少温室气体CO2的排放,科学家将CO2和H2在催化剂和加热的条件下反应,转化为水和甲烷,该反应的化学方程式为 .有人说:“空气中CO2的含量越少越好”,你是否同意这种说法(填“是”或“否”) ,理由是 . (5)金刚石和石墨的物理性质差异较大,主要原因是 . (6)在工业上可利用CO和NaOH通过化合反应制备HCOONa(甲酸钠),该反应的化学方程式为 . 【答案】 (1)CO2 (2)CO2+Ca(OH)2═CaCO3↓+H2O (3)CH4+2O2 (4)CO2+4H2 (5)碳原子的排列方式不同 (6)CO+NaOH 10.(2017荆门化学)(1)如图1是a、b、c三种物质的溶解度曲线,回答下列问题: ①t2℃时,a、b、c三种物质的溶解度由大到小的顺序为 . ②P点的含义是 . ③t2℃时,将40ga物质加入50g水中,充分溶解后得到溶液的质量为 g. ④将a、b、c三种物质的饱和溶液从t2℃降温到t1℃时,溶液中溶质的质量分数不变的是 . (2)A﹣G是初中化学常见物质,A、C在常温下是气体且元素组成相同,B是铁锈的主要成分,E的相对分子质量为100,它们的相互转化关系如图2(部分反应物、生成物 ①写出物质E的化学式 . ②写出有关反应的化学方程式: (Ⅰ)A+B→ ; (Ⅱ)G+Na2CO3溶液→ . ③写出F的一种用途 . 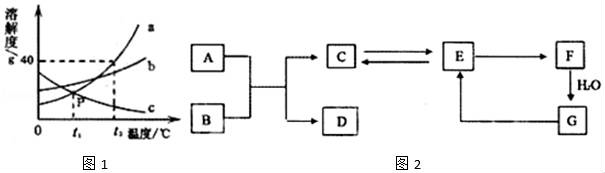 【答案】 (1)①a>b>c ②t1℃时,a、c物质的溶解度相等 ③70 ④c (2)①CaCO3 ②(Ⅰ)3CO+Fe2O3 (Ⅱ)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH ③干燥剂 三、(2017荆门化学)实验探究 11.在探究金属活动性的实验课上,同学们把打磨光亮的铝片插入硫酸铜溶液中,过一会儿,发现了一个“意外现象”:在铝片表面看到有红色固体析出的同时,还看到有少量的气泡冒出,写出生成红色固体的化学方程式 . 【提出问题】该气体是什么呢? 【猜想与假设】猜想一:O2 猜想二:H2 猜想三:CO2 猜想四:SO2 同学们经过讨论,一致认为猜想三不成立,理由是 【实验验证】 1、有同学闻了一下该气体,发现无气味,证明猜想四也不成立,理由是 . 2、将产生的气体经验纯后,用导管导入到点燃的酒精灯火焰上,气体安静燃烧,产生淡蓝色火焰. 【实验结论】 . 【反思与交流】CuSO4溶液可能显 【答案】 2Al+3CuSO4=3Cu+Al2(SO4)3 反应物中不含碳元素 二氧化硫有刺激性气味 猜想一不成立,猜想二成立 酸 四、(2017荆门化学)计算题. 12.为测定某黄铜(铜、锌合金)中铜的质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
(1)完全反应后生成氢气的质量为 g. (2)计算该黄铜中铜的质量分数(写出计算过程). 根据质 设参加反应的锌的质量为x. Zn+H2SO4=ZnSO4+H2↑ 65 2 x 0.4g x=13g 该黄铜中铜的质量分数为 答:(1)完全反应后生成氢气的质量为0.4g. (2)该黄铜中铜的质量分数为60%. (责任编辑:admin) |
