|
北京市2008─2009学年度第二学期初三统一练习 计算题汇编 司志书(供稿) 1.(崇文)现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成。 【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入到该烧杯中,充分反应后,测得剩余固体质量的数据记录如下:
通过计算(写出计算过程,结果精确到0.1%),求: (1)该混合物粉末中铜的质量分数? (2)该混合物粉末中另一金属为何种金属? (3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少? 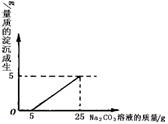 2.(门头沟)刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数。他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示。(Na2CO3+CaCl2= CaCO3↓+2NaCl) 2.(门头沟)刘明用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数。他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示。(Na2CO3+CaCl2= CaCO3↓+2NaCl)(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质除含有CaCl2外,还含有______________________; (2)计算Na2CO3溶液中溶质的质量分数。(计算结果精确到0.1%) 3.(怀柔)某品牌纯碱产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验;取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,充分反应后,实验数据记录如下:
请你据此分析计算: (1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。 (2)该产品中碳酸钠的质量分数? 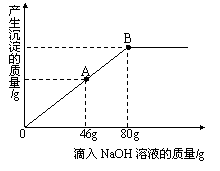 4.(朝阳)向盛有102 g不饱和硫酸镁溶液的烧杯中,逐滴滴入溶质质量分数为10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液的质量关系曲线如图所示。 4.(朝阳)向盛有102 g不饱和硫酸镁溶液的烧杯中,逐滴滴入溶质质量分数为10%的NaOH溶液,产生沉淀的质量与所滴入NaOH溶液的质量关系曲线如图所示。请根据题意回答下列问题: 反应方程式为:MgSO4 + 2NaOH == Na2SO4 + Mg(OH)2↓ (1)当滴入NaOH溶液至图中A点时,烧杯中溶液里 含有的溶质是(写化学式) 。 (2)当滴入10%的NaOH溶液80g时(即B点),试通过 计算,求此时所得溶液中溶质的质量分数。 5(海淀).长期使用热水瓶底部或热水器中有水垢,主要成分是碳酸钙和氢氧化镁(假设无其它杂质)。某课外小组想测定水垢中碳酸钙的含量,他们取20.8g水垢,加入足量的浓度为14.6%的盐酸,其中产生的二氧化碳的数据见下表。
计算:(1)水垢中碳酸钙的质量分数 。 (2)要使水垢完全溶解,最少需要盐酸的质量 。 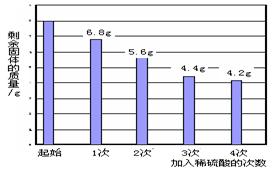 6.(昌平)现有铜与金属镁、铁、锌中的一种组成的混合物,现欲测定其组成。 【查阅资料】镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属化合物和氢气。 【实验步骤及数据】取该混合物粉末8.0 g放入烧杯中,将140.0 g 绒织的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图: 通过计算(写出计算过程),求: (1)该混合物粉末中铜的质量分数? (2)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少? 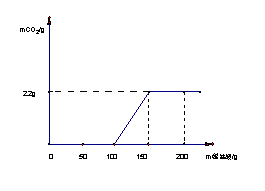 7.(平谷)(3分)为测定某变质烧碱样品中NaOH的质量分数,取一定量的该烧碱样品于试管中,向样品中逐滴加入过量的稀盐酸,产生的气体与所加入稀盐酸质量关系如下图所示: 7.(平谷)(3分)为测定某变质烧碱样品中NaOH的质量分数,取一定量的该烧碱样品于试管中,向样品中逐滴加入过量的稀盐酸,产生的气体与所加入稀盐酸质量关系如下图所示:(1)计算该烧碱样品中氢氧化钠的质量分数。 (2)求样品与稀盐酸恰好反应时所得溶液中 溶质的质量分数为多少?
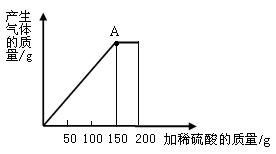 请计算: (1)a的数值为 。 (2)合金中铜的质量分数为 。 (3)实验所用稀硫酸的质量分数是 。 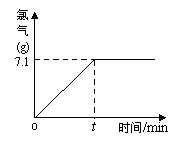 10(通州).(3分)氯化钠除了用做调味品外,还是一种重要的化工原料。氯碱厂用给氯化钠溶液通电的方法可制得氢氧化钠、氯气和氢气。某实验小组同 10(通州).(3分)氯化钠除了用做调味品外,还是一种重要的化工原料。氯碱厂用给氯化钠溶液通电的方法可制得氢氧化钠、氯气和氢气。某实验小组同学在老师帮助下,取一定质量含氯化钠质量分数为10% 的溶液进行电解,当氯化钠完全反应后,停止通电。右 图是他们对生成的氯气质量与时间关系所做的分析记录。 试计算: (1)参加反应的氯化钠质量是多少? (2)完全反应后所得溶液的质量分数是多少? 11.(延庆) (3分)化学实验小组的同学们通过查阅资料了解到:酸和碱反应时有放热现象。他们将不同溶质质量分数的盐酸和氢氧化钠溶液各10 g混合,用温度计测定混合前后温度的升高值△t,记录如下:
(1)表中x =________________。 (2)计算第2组实验后,得到的溶液中溶质的质量分数。 (3)为了保护环境,实验结束后,同学们将各组实验后产生的废液汇集在一起进行处理。请分析该废液的酸碱性,若不是中性溶液,请选用第1组实验中提供的试剂进行处理,将溶液调至中性。你选的试剂及其用量是_________。 (责任编辑:admin) |

 8.(石景山)(3分)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成。某同学进行了如下实验:称量8.0 g该混合物粉末放入烧杯中→将140 g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图。试计算:
8.(石景山)(3分)为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成。某同学进行了如下实验:称量8.0 g该混合物粉末放入烧杯中→将140 g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图。试计算: